Nuevo punto crítico del agua: el hallazgo que explica sus propiedades más extrañas
Un experimento sin precedentes ha permitido observar el comportamiento oculto del agua en condiciones extremas para desentrañar un fenómeno clave que llevaba décadas siendo solo una hipótesis. El descubrimiento de un nuevo punto crítico ayuda a explicar por qué el agua, esencial para la vida, se comporta de forma tan extraordinaria frente a cualquier otro líquido.
Por Enrique Coperías, periodista científico
Un haz láser atraviesa un vaso de agua en esta recreación conceptual que ilustra cómo las técnicas con rayos X permiten observar la estructura molecular del agua en condiciones extremas, clave para descubrir su nuevo punto crítico. Cortesía: POSTECH University, South Korea
El agua, esa sustancia cotidiana que cubre la mayor parte del planeta y hace posible la vida, sigue guardando secretos capaces de desconcertar a la ciencia más avanzada.
Prueba de ello es que un equipo de investigadores de la Universidad de Estocolmo, en Suecia, ha logrado ahora observar experimentalmente un fenómeno que hasta ahora solo era teórico: un nuevo punto crítico en agua sobreenfriada, situado en torno a los -63 °C y a unas mil atmósferas de presión.
El hallazgo, publicado en la revista Science, aporta una pieza clave para explicar por qué el agua se comporta de forma tan extraña frente a otros líquidos.
Por qué el agua es un líquido único
A diferencia de la mayoría de las sustancias, el agua desafía las reglas básicas de la física cotidiana. Lo habitual es que la materia se contraiga al enfriarse y aumente su densidad. Sin embargo, el agua alcanza su máxima densidad a los 4 °C. Por debajo de esa temperatura, en lugar de seguir contrayéndose, comienza a expandirse, un fenómeno que explica por qué el hielo flota.
Este comportamiento anómalo se extiende a otras propiedades, como la compresibilidad o la capacidad calorífica, que se vuelven cada vez más inusuales a medida que desciende la temperatura. Recordemos que la compresibilidad es la facilidad con la que una sustancia puede reducir su volumen cuando se le aplica presión. En el agua, cambia de forma poco habitual según la temperatura.
Por su parte, la capacidad calorífica es la cantidad de calor que una sustancia puede absorber antes de aumentar su temperatura. El agua tiene una capacidad calorífica muy alta, por eso tarda en calentarse y enfriarse.
La clave: dos formas líquidas del agua
Pues bien, desde hace tiempo los científicos han tratado de explicar sin éxito estas rarezas mediante teorías que apuntaban a la existencia de dos formas líquidas distintas del agua en condiciones extremas: una más densa y otra menos densa. Según esa hipótesis, ambas fases convergerían en un punto crítico en el régimen de agua profundamente sobreenfriada.
Sin embargo, demostrarlo experimentalmente había resultado hasta ahora imposible.
El avance ha sido posible gracias al uso de pulsos ultracortos de rayos X generados por láseres de rayos X, que permiten observar el agua antes de que se congele.
🗣️ «Lo especial de nuestro ensayo fue que pudimos hacer radiografías a una velocidad inimaginable antes de que el hielo se formara, y observar cómo la transición líquido-líquido desaparece y emerge un nuevo estado crítico —explica Anders Nilsson, profesor de Física Química en la Universidad de Estocolmo. Y añade—: Durante décadas ha habido especulaciones y diferentes teorías para explicar estas propiedades tan notables, y una de ellas era la existencia de un punto crítico. Ahora hemos encontrado que ese punto existe».
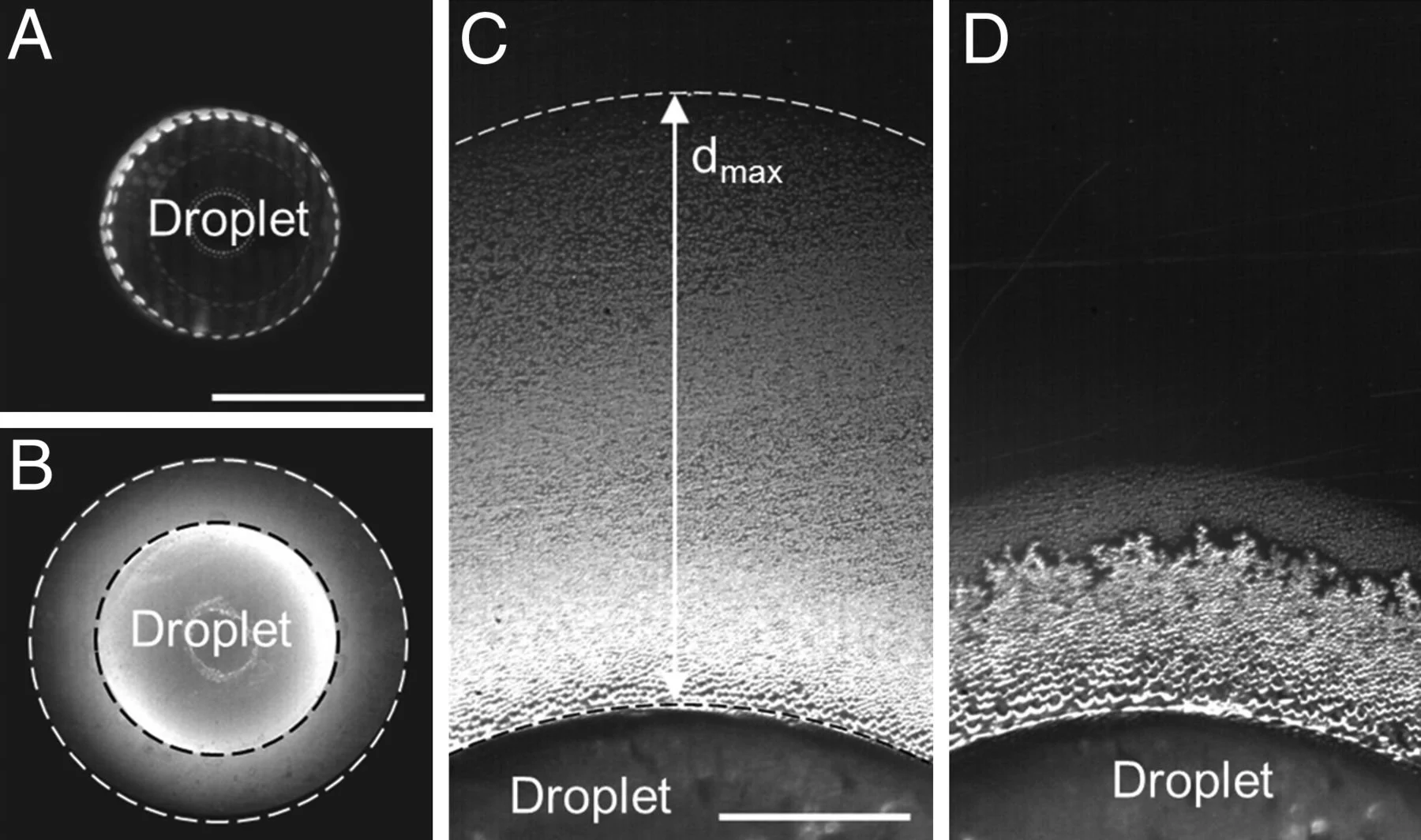
Halo de condensación alrededor de una gota de agua sobreenfriada durante su congelación, observado con microscopía óptica. La imagen muestra cómo el vapor se difunde y se condensa en un anillo brillante alrededor de la gota, revelando procesos físicos clave en condiciones extremas que ayudan a entender el comportamiento del agua cerca de su punto crítico. Cortesía: S. Jung, M. K. Tiwari & D. Poulikakos
Qué es un punto crítico en el agua
El descubrimiento confirma que, en condiciones de baja temperatura y alta presión, el agua puede existir en dos estados líquidos macroscópicos con diferentes estructuras de enlace entre sus moléculas.
A medida que aumenta la temperatura y disminuye la presión, la distinción entre ambas fases se difumina hasta desaparecer en ese punto crítico, una región de gran inestabilidad donde las fluctuaciones se extienden incluso hasta condiciones ambientales.
En ese régimen, el agua oscila entre ambas configuraciones «como si no pudiera decidirse» por una de ellas, y son esas fluctuaciones las que originan sus propiedades anómalas. Más allá de ese punto, el agua entra en un estado supercrítico, en el que se encuentra, de hecho, el agua en condiciones habituales.
Un comportamiento casi «imposible del que escapar»
El estudio también ha revelado un comportamiento dinámico inesperado. «Parece casi que no puedes escapar del punto crítico si entras en él; es casi como un agujero negro», señala Robin Tyburski, investigador en Física Química en la misma universidad.
Para el equipo, el camino hasta este resultado ha sido tan sorprendente como el propio hallazgo.
🗣️ «Es asombroso cómo los hielos amorfos, un estado del agua tan ampliamente estudiado, han resultado ser nuestra puerta de entrada a la región crítica. Es una gran inspiración para mis futuras investigaciones y un recordatorio de las posibilidades de hacer descubrimientos en temas tan estudiados como el agua», afirma Aigerim Karina, investigadora posdoctoral y coautora del estudio.
No hay que olvidar que los llamados hielos amorfos han resultado ser una pieza clave para explorar este comportamiento esquivo del agua. A diferencia del hielo convencional, donde las moléculas se organizan en una estructura cristalina ordenada, en estos estados amorfos quedan dispuestas de forma desordenada, como en un vidrio congelado. Este carácter caótico permite a los investigadores estudiar el agua en condiciones extremas —como temperaturas muy bajas o presiones elevadas— sin que llegue a cristalizar, abriendo así una ventana única para observar fenómenos como el punto crítico ahora identificado.
Un reto experimental histórico
El reto experimental tampoco ha sido menor. «Fue un sueño hecho realidad poder medir el agua en condiciones de temperatura extremadamente baja sin que se congelara —recuerda Iason Andronis, doctorando en Física Química—. Muchos habían soñado con encontrar este punto crítico, pero los medios no habían estado disponibles antes del desarrollo de los láseres de rayos X».
Más allá de la física fundamental, el descubrimiento abre interrogantes de mayor alcance.
🗣️ «Me parece muy emocionante que el agua sea el único líquido supercrítico en condiciones ambientales donde existe la vida, y también sabemos que no hay vida sin agua. ¿Es una pura coincidencia o hay algún conocimiento esencial que podamos obtener en el futuro?», plantea Fivos Perakis, profesor de Física Química que ha colaborado en este trabajo.
Un debate científico con más de un siglo
El hallazgo podría ayudar a resolver un debate que se remonta a más de un siglo. «Ha habido una intensa discusión sobre el origen de las propiedades extrañas del agua desde los primeros trabajos de Wolfgang Röntgen — recuerda Nilsson. Y concluye—: Los investigadores que estudian la física del agua pueden ahora asentarse en el modelo de que el agua tiene un punto crítico en el régimen sobreenfriado. El siguiente paso es encontrar las implicaciones de estos resultados en procesos físicos, químicos, biológicos, geológicos y climáticos. Un gran desafío para los próximos años».
El estudio ha contado con la colaboración de instituciones de Corea del Sur, Alemania y Canadá, en un esfuerzo internacional que demuestra que incluso las sustancias más familiares pueden seguir escondiendo fenómenos inesperados.
En el caso del agua, ese misterio no solo es fascinante: también podría ser clave para entender mejor el mundo que habitamos.▪️(28-marzo-2026)
PREGUNTAS&RESPUESTAS: Agua y Estados
💦 ¿Qué es el agua sobreenfriada?
Es agua líquida que permanece en estado líquido por debajo de 0 °C sin congelarse.
💦 ¿Por qué es importante este descubrimiento?
Porque explica las propiedades anómalas del agua, fundamentales para procesos naturales y la vida.
💦 ¿Dónde se publicó el estudio?
En la revista científica Science.
💦 ¿Qué tecnología permitió el hallazgo?
Láseres de rayos X con pulsos ultrarrápidos.
💦 ¿Afecta esto al agua que usamos a diario?
Sí, indirectamente: las propiedades del agua cotidiana están influenciadas por este punto crítico.
FÍSICA Y MECÁNICA CUÁNTICA
Información facilitada por la Universidad de Estocolmo
Fuente: Seonju You et al. Experimental evidence of a liquid-liquid critical point in supercooled water.Science(2026). DOI:10.1126/science.aec0018