Autofagia y ELA: un fallo en la «limpieza celular» abre nuevas vías terapéuticas contra la esclerosis lateral amiotrófica
Un mecanismo fundamental que permite a las neuronas eliminar proteínas tóxicas falla en la ELA, lo que acelera su degeneración. El hallazgo, observado en tejido humano, apunta a una nueva estrategia para frenar la enfermedad desde dentro de la célula.
Por Enrique Coperías, periodista científico
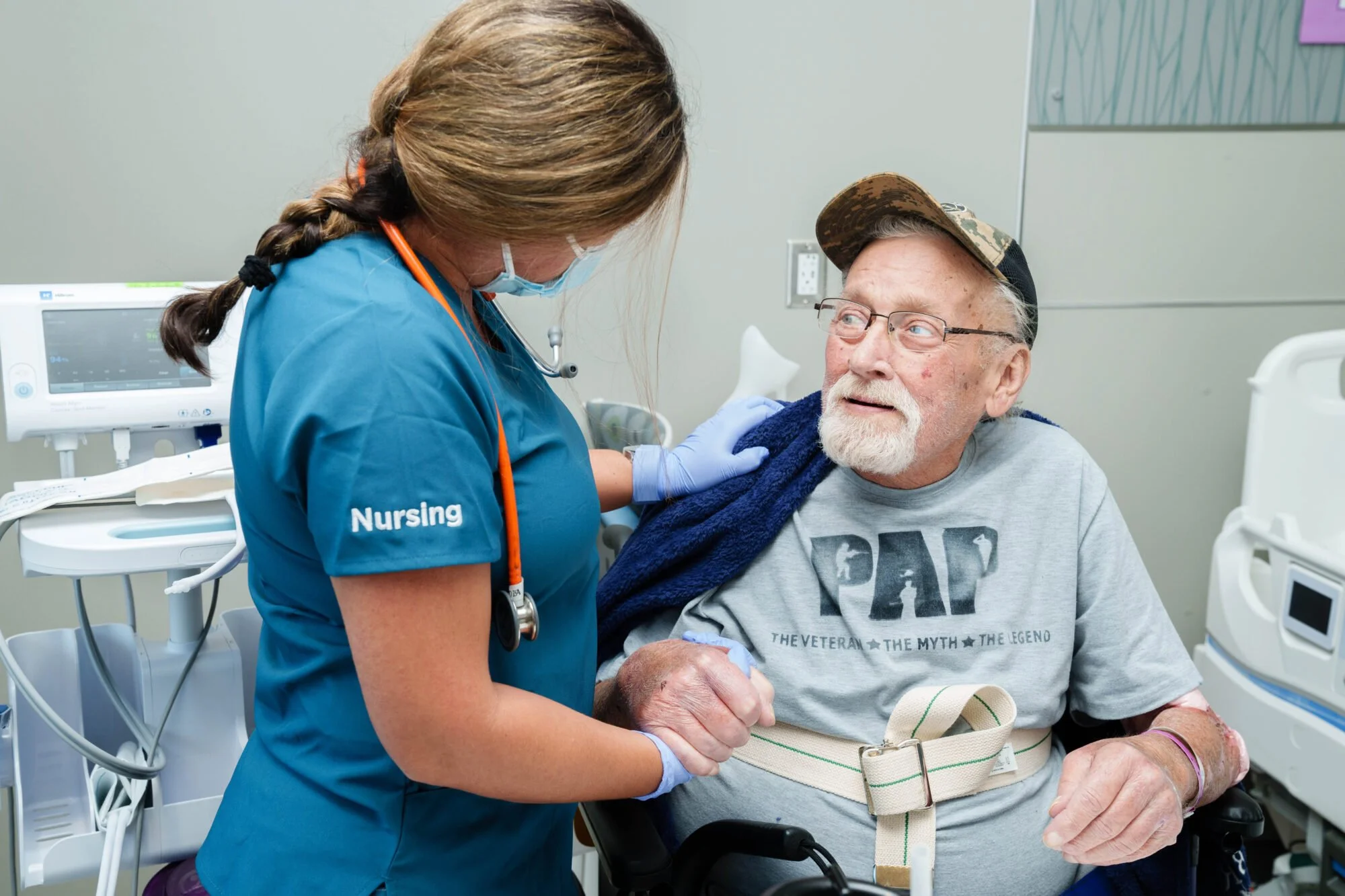
Una profesional sanitaria atiende a un paciente, reflejo del impacto clínico de la ELA, una enfermedad que provoca la pérdida progresiva de las neuronas motoras y para la que nuevas vías terapéuticas, como la autofagia mediada por chaperonas, empiezan a abrirse paso. Cortesía: Bbrooks Rehabilitation
¿Qué es la ELA y por qué sigue siendo un desafío?
La esclerosis lateral amiotrófica (ELA) sigue siendo uno de los grandes enigmas de la medicina contemporánea. Se trata de una enfermedad devastadora: las neuronas motoras, encargadas de transmitir las órdenes del cerebro a los músculos, se deterioran progresivamente hasta provocar parálisis y, finalmente, la muerte en pocos años.
Desde el punto de vista epidemiológico, la ELA es una enfermedad poco frecuente pero de gran impacto: cada año se diagnostican entre 1,5 y 2 nuevos casos por cada 100.000 habitantes, lo que equivale a unos tres diagnósticos diarios en España. Su prevalencia, o sea, el número total de personas afectadas, se sitúa entre tres y cinco casos por cada 100.000 habitantes, lo que se traduce en alrededor de 4.000 pacientes en nuestro país. Por ello, está considerada una enfermedad rara o minoritaria.
En aproximadamente el 90 % de los casos, la ELA aparece de forma esporádica, sin antecedentes familiares conocidos. El 10 % restante corresponde a formas hereditarias, generalmente transmitidas con un patrón dominante. En los últimos años, los avances en genética molecular han permitido identificar más de veinticinco genes implicados en la enfermedad, lo que ha abierto nuevas vías para comprender sus causas y desarrollar futuras terapias.
El hallazgo: un fallo en la autofagia mediada por chaperonas
Pero a pesar de décadas de investigación, los tratamientos disponibles apenas logran retrasar el curso de la enfermedad. En este contexto, cada nuevo hallazgo sobre sus mecanismos íntimos se recibe como una posible puerta de entrada a terapias más eficaces. No es casual pues que los propios investigadores subrayen la magnitud del desafío:.
🗣️ «La ELA es una enfermedad devastadora cuya causa sigue siendo desconocida en la gran mayoría de los pacientes, lo que dificulta enormemente el desarrollo de tratamientos eficaces», explica el catedrático de la Universidad Miguel Hernández (UMH) Salvador Martínez, director del laboratorio Neurobiología de las Enfermedades Mentales, Neurodegenerativas y Neurooncológicas, en Alicante (España).
Un estudio, publicado en la revista Acta Neuropathologica Communications, aporta una pieza clave a ese rompecabezas. El trabajo, liderado por investigadores españoles, identifica un fallo específico en un sistema celular de limpieza, la llamada autofagia mediada por chaperonas, como un factor determinante en la degeneración de las neuronas motoras en la ELA esporádica, la forma más común de la enfermedad.
Recordemos que laschaperonas son proteínas que ayudan a otras proteínas a plegarse correctamente y a mantener su estructura, evitando que se dañen o se acumulen de forma tóxica en la célula.
Este avance, señalan sus autores, apunta directamente a nuevas estrategias: «Identificar mecanismos celulares implicados directamente en la supervivencia de las neuronas es un paso fundamental para avanzar en nuevas estrategias terapéuticas», comenta Martínez.
¿Qué han descubierto los investigadores?
Uno de los rasgos distintivos de la ELA es la acumulación de proteínas anómalas dentro de las neuronas. En concreto, la proteína TDP-43, que en condiciones normales desempeña funciones esenciales en el procesamiento del ARN, aparece mal localizada y forma agregados tóxicos en el citoplasma celular. Este fenómeno se observa en alrededor del 95 % de los casos.
Las células disponen de varios sistemas para eliminar estas proteínas defectuosas. Entre ellos destaca la autofagia, un proceso mediante el cual los componentes dañados se degradan en estructuras llamadas lisosomas. Pero la autofagia no es un mecanismo único: existen distintas variantes. La más conocida es la macroautofagia, que actúa como un sistema de limpieza a gran escala. Sin embargo, hay otra vía más selectiva y menos estudiada: la autofagia mediada por chaperonas (CMA).
Esta última funciona como un sistema de recogida selectiva. Proteínas específicas son reconocidas por unas moléculas auxiliares —las chaperonas— que las conducen hasta los lisosomas, que, dicho sea de paso, se trata de unos orgánulos celulares esféricos, formados por el aparato de Golgi, que actúan como el sistema digestivo de la célula.
Allí, un receptor clave, llamado LAMP2A, permite su entrada y posterior degradación. Si este mecanismo falla, las proteínas dañadas pueden acumularse allí donde no deben hacerlo.
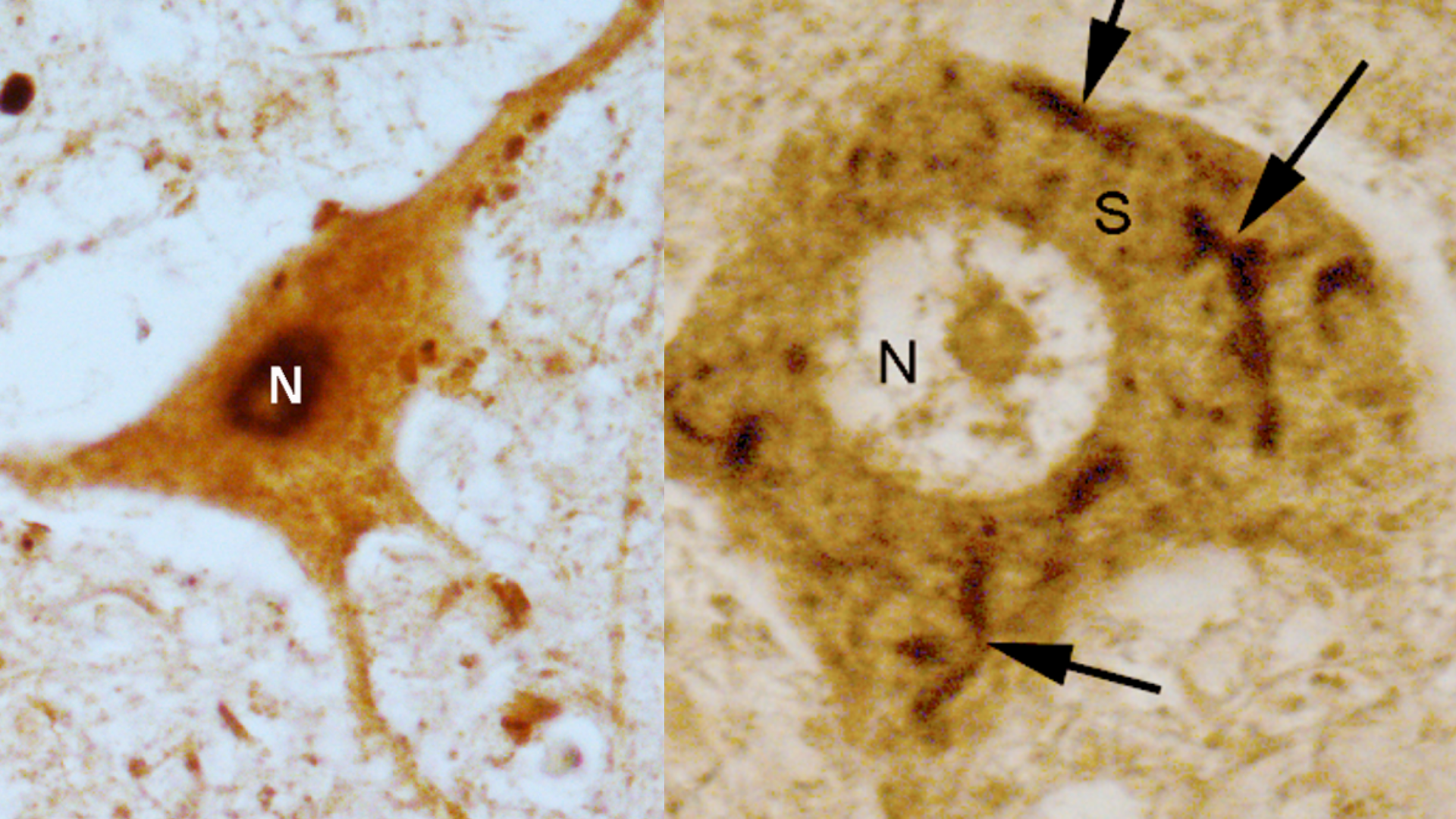
Motoneuronas de la médula espinal: a la izquierda, una neurona sana en la que la proteína TDP-43 (en negro) se localiza en el núcleo (N); a la derecha, una neurona de un paciente con ELA, donde TDP-43 se acumula de forma anómala en el citoplasma del cuerpo celular (S), un rasgo característico de la enfermedad. Cortesía: Instituto de Neurociencias UMH / CSIC
Una pista en la médula espinal
El estudio se centra en la médula espinal humana, donde residen muchas de las neuronas motoras afectadas en la ELA. Los investigadores analizaron muestras de tejido de pacientes y las compararon con controles sanos. El objetivo era comprobar si la autofagia mediada por chaperonas funcionaba de forma correcta.
El hallazgo principal es contundente: en las neuronas motoras de los pacientes con ELA esporádica, la actividad de la autofagia mediada por chaperonas está claramente reducida. Esto se evidenció por la disminución de la LAMP2A, el receptor esencial de este sistema, cuya presencia es un indicador directo de su funcionamiento.
➡️ En palabras del investigador Daniel Garrigós García, primer autor del trabajo, «estos datos indican que la actividad de la autofagia mediada por chaperonas está claramente disminuida en las neuronas motoras de los pacientes con ELA».
En las muestras sanas, las neuronas motoras mostraban niveles elevados de LAMP2A, lo que sugiere que estas células dependen especialmente de este mecanismo para mantener su equilibrio celular. En cambio, en las neuronas de pacientes, esos niveles eran mucho más bajos, coincidiendo con la acumulación de TDP-43.
Este resultado sugiere una relación directa: cuando falla la CMA, la proteína TDP-43 no se elimina correctamente y se acumula, contribuyendo al daño neuronal que se observa en la esclerosis lateral amniotrófica.
Un fallo selectivo
Uno de los aspectos más llamativos del estudio es que no todos los sistemas de limpieza celular parecen afectados. Los investigadores analizaron también la macroautofagia, utilizando marcadores como la proteína LC3, y no encontraron diferencias significativas entre pacientes y controles.
Esto indica que el problema no es un colapso general de la capacidad de la célula para degradar proteínas, sino un defecto específico en la autofagia mediada por chaperonas. Es decir, el sistema más selectivo, el que actúa como un control de calidad fino, es el que falla.
Esta especificidad podría explicar por qué ciertas proteínas, como TDP-43, se acumulan de forma tan característica en la ELA, mientras que otros componentes celulares permanecen relativamente intactos.
Neuronas resistentes: la pista del núcleo de Onuf
La ELA no afecta a todas las neuronas por igual. Algunas poblaciones neuronales son sorprendentemente resistentes a la degeneración neuronal. El nuevo trabajo arroja luz sobre esta cuestión al analizar un grupo particular de neuronas: las del núcleo de Onuf, implicadas en funciones como el control de esfínteres.
Estas neuronas suelen preservarse incluso en fases avanzadas de la enfermedad. ¿Por qué? Según los resultados, mantienen niveles normales de LAMP2A y no presentan acumulación de TDP-43.
Este hallazgo sugiere que la integridad de la autofagia mediada por chaperonas podría ser un factor clave que protege a determinadas neuronas frente a la degeneración. En otras palabras, no todas las neuronas son igual de vulnerables porque no todas dependen del mismo modo de este sistema de limpieza.
🗣️ «En nuestro artículo hemos descrito que las motoneuronas necesitan niveles muy altos de autofagia mediada por chaperonas para sobrevivir. Cuando este mecanismo disminuye, como ocurre en la ELA, son precisamente estas células las que primero sufren y acaban muriendo», resume Martínez.
Inflamación y respuesta glial
El estudio también observa un fenómeno complementario: mientras que las neuronas motoras pierden actividad de la CMA, ciertas células gliales —las células de soporte del sistema nervioso— muestran un aumento de LAMP2A.
Este incremento podría estar relacionado con procesos inflamatorios asociados a la enfermedad.
Las células gliales reaccionan al daño neuronal y podrían activar sus mecanismos de limpieza como respuesta al estrés celular. Sin embargo, esta activación no parece suficiente para compensar el fallo en las neuronas motoras.
Implicaciones terapéuticas: una nueva diana contra la ELA
Más allá de la descripción del problema, el trabajo apunta hacia una posible solución. Si la disminución de la autofagia mediada por chaperonas contribuye a la acumulación de proteínas tóxicas, entonces potenciar este sistema podría tener efectos beneficiosos.
Los autores plantean que aumentar la actividad de LAMP2A y, por tanto, de la CMA, podría ayudar a restaurar el equilibrio proteico en las neuronas motoras. Esto abriría una nueva línea de investigación terapéutica, centrada no tanto en eliminar los síntomas como en corregir uno de los mecanismos fundamentales de la enfermedad. «Nuestro objetivo es intentar modular esta vía para aumentar su actividad», señala Martínez.
Aunque aún se trata de una hipótesis, la idea encaja con otros estudios que han mostrado que mejorar los sistemas de degradación celular puede reducir la toxicidad de proteínas como TDP-43.
Imagen de diagnóstico neurológico: la investigación en ELA avanza hacia el estudio de mecanismos celulares como la eliminación selectiva de proteínas, clave para entender la acumulación tóxica de TDP-43 y la degeneración neuronal. Foto de Vitaly Gariev en Unsplash
Un avance en un terreno complejo
La ELA es una enfermedad heterogénea, con múltiples factores implicados. Solo un pequeño porcentaje de los casos, como ya se ha adelantado, tiene un origen genético claro; la mayoría son esporádicos y de causa desconocida. Esto complica enormemente el desarrollo de tratamientos.
En este contexto, identificar un mecanismo celular concreto, como el fallo de la autofagia mediada por chaperonas, supone un avance significativo. No solo ayuda a entender mejor por qué mueren las neuronas motoras, sino que proporciona un objetivo específico para futuras terapias.
Además, el estudio refuerza una idea cada vez más aceptada en neurociencia: que el equilibrio en la gestión de proteínas —la llamada proteostasis— es crucial para la supervivencia neuronal. Cuando ese equilibrio se rompe, las consecuencias pueden ser devastadoras. Como subraya el propio equipo, el avance metodológico también es relevante: «Hemos podido observar este mecanismo directamente en tejido humano, algo que no habíamos logrado en modelos animales», destaca Martínez.
Hacia una nueva comprensión de la ELA
Queda mucho por investigar. Será necesario confirmar estos hallazgos en estudios más amplios y explorar cómo se puede intervenir sobre la autofagia mediada por chaperonas de forma segura y eficaz. También habrá que entender por qué este sistema falla en unas neuronas y no en otras, y cómo se relaciona con otros procesos implicados en la ELA.
Pero el camino está trazado. En un campo donde los avances han sido lentos y los fracasos frecuentes, cada nueva pista cuenta. Este trabajo no ofrece una cura, pero sí una dirección clara: mirar hacia los mecanismos internos de limpieza celular como una posible clave para frenar la degeneración neuronal.
En la lucha contra la ELA, comprender cómo y por qué fallan nuestras propias células puede ser el primer paso para aprender a protegerlas.▪️(30-abril-2026)
ENFERMEDADES NEURODEGENERATIVAS
PREGUNTAS&RESPUESTAS: ELA y Autofagia
🩺 ¿Qué causa la ELA?
En la mayoría de los casos, la causa es desconocida. Se cree que intervienen factores genéticos y ambientales.
🩺 ¿Qué es la autofagia?
Es el sistema de reciclaje celular que elimina componentes dañados.
🩺 ¿Qué diferencia hay entre CMA y macroautofagia?
Macroautofagia: elimina grandes cantidades de material
CMA: elimina proteínas específicas de forma selectiva
🩺 ¿Por qué es importante la proteína TDP-43?
Porque su acumulación tóxica está presente en la mayoría de los pacientes con ELA.
🩺 ¿Este descubrimiento puede curar la ELA?
No todavía, pero identifica una nueva diana terapéutica prometedora.
Información facilitada por la Universidad Miguel Hernández
Fuente: Garrigos, D., Martinez-Morga, M., Pombero, A. et al.Chaperone mediated autophagy is deficient in spinal motoneurons of ALS patients with TDP-43 proteinopathy. Acta Neuropathologica Communications (2026). DOI: https://doi.org/10.1186/s40478-026-02238-6