El legado oculto del ADN denisovano: cómo nuestros ancestros nos ayudaron a resistir enfermedades tropicales
Un linaje humano extinguido hace miles de años sigue vivo en nosotros: fragmentos de su ADN refuerzan nuestras defensas. El legado de los denisovanos explica por qué algunas poblaciones resisten mejor a la malaria y a otras enfermedades tropicales.
Por Enrique Coperías
Recreación artística de los denisovanos en la Cobra Cave de Laos, un entorno tropical donde su sistema inmunitario se forjó frente a mosquitos, parásitos y virus. Esa adaptación genética, transmitida después a Homo sapiens, aún protege a poblaciones actuales frente a enfermedades tropicales. IMagen generada con DALL-E
Hace apenas quince años, el hallazgo de un diminuto fragmento de hueso en la cueva siberiana de Denisova, en las montañas de Altái, cambió para siempre la manera en que entendemos la historia de nuestra especie. Aquel hueso no pertenecía ni a un neandertal ni a un humano moderno, sino a un grupo hasta entonces desconocido: los denisovanos.
Desde entonces, las investigaciones genéticas apuntan a que este linaje humano, que convivió e incluso se mezcló con Homo sapiens y neandertales, dejó una huella indeleble en nuestro ADN. Y no se trata de un mero vestigio arqueológico escondido en las cadenas de nucleótidos, sino de una herencia genética viva que todavía condiciona cómo respondemos a nuestro entorno.
Un nuevo estudio científico acaba de demostrar que algunos fragmentos de ADN denisovano nos protegen frente a enfermedades tropicales que, de otro modo, habrían sido letales para nuestros ancestros y que siguen representando un desafío en la actualidad.
Denisovanos: de Siberia a los trópicos
La paradoja es evidente: los denisovanos confirmados por restos fósiles habitaron cuevas en Siberia y en el altiplano tibetano, territorios fríos, de inviernos largos y climas extremos que poco tienen que ver con las selvas húmedas de Melanesia o Filipinas, donde hoy encontramos la mayor proporción de su legado genético.
👉 Pero ¿cómo explicar entonces que esas variantes heredadas hayan acabado ayudando a poblaciones humanas a resistir la malaria o la leishmaniasis? La respuesta, según la investigación, reside en que los denisovanos no fueron un grupo homogéneo ni limitado a unas pocas cuevas.
En algún momento de su historia, también ocuparon regiones tropicales, como demuestra el hallazgo de un molar en la llamada Cobra Cave, en Laos. Allí, hace unos 160.000 años, vivieron en un ambiente de bosques húmedos y estaciones de lluvias intensas, expuestos a mosquitos, parásitos intestinales y virus transmitidos por murciélagos. Fue en esos escenarios donde su sistema inmunitario se forjó frente a amenazas que, siglos después, resultarían decisivas para los humanos modernos.
La situación especial de los denisovanos de Laos
El estudio, liderado por Attila Trajer, del Laboratorio de Investigación de Soluciones de Sostenibilidad, en la Universidad de Panonia (Hungría), y publicado en la revista Journal of Human Evolution, combina reconstrucciones climáticas del pasado con el análisis de la distribución actual de agentes patógenos y las huellas genéticas denisovanas en poblaciones humanas.
El resultado es un mapa evolutivo en el que se cruzan biomas, enfermedades y genes. Los autores constatan que mientras las cuevas de Siberia y del Tíbet ofrecían pocos escenarios favorables para parásitos tropicales, el entorno de Laos presentaba condiciones idóneas para Plasmodium vivax, el parásito de la malaria; para helmintos, como la lombriz intestinal Ascaris lumbricoides, que causa la ascariasis; para mosquitos del género Anopheles; e incluso para el virus Nipah, transmitido por murciélagos frugívoros.
En otras palabras: los denisovanos de esta región se enfrentaron a un paisaje microbiano muy parecido al que hoy amenaza a millones de personas en el sudeste asiático y Oceanía.
ADN denisovano y resistencia a enfermedades
Ese contacto prolongado con ciertos agentes patógenos dejó una huella en su ADN. Cuando el Homo sapiens salió de África y se encontró con los denisovanos hace unos 50.000 años, no solo se mezclaron cultural y biológicamente: también recibieron un paquete de supervivencia en forma de genes adaptados a entornos desconocidos.
Algunas de esas variantes todavía hoy están presentes en poblaciones de Papúa Nueva Guinea, Filipinas o Vanuatu, donde el porcentaje de herencia denisovana llega a superar el 5% del genoma. Los investigadores apuntan a ejemplos concretos. Genes inmunitarios de la familia de los receptores tipo Toll (TLR1 y TLR6) y de las enzimas OAS (oligoadenilato sintetasa), esenciales en la respuesta antiviral, muestran claros indicios de haber sido heredados de homínidos arcaicos y de haber pasado por un proceso de selección positiva.
Lo mismo ocurre con el alelo T108A;I207L, relacionado con una mayor activación del sistema inmunitario, especialmente útil frente a infecciones intestinales o transmitidas por mosquitos, aunque con la contrapartida de aumentar el riesgo de enfermedades autoinmunes.
👉 La paradoja de esta herencia genética es que lo que ayer fue salvación, hoy puede ser un problema. La misma mutación que ayudaba a combatir parásitos en los trópicos puede desencadenar en la actualidad cuadros de psoriasis, artritis o lupus en contextos donde la presión infecciosa es menor. Es un delicado equilibrio entre beneficio y coste, típico de la evolución humana: la selección natural favorece lo útil en un momento y lugar concretos, aunque a largo plazo pueda generar efectos secundarios.
El estudio menciona también la deleción LCE3BC, heredada de denisovanos, que aumenta la respuesta inmunitaria frente a infecciones pero está asociada con trastornos inflamatorios de la piel. De nuevo, un arma de doble filo.
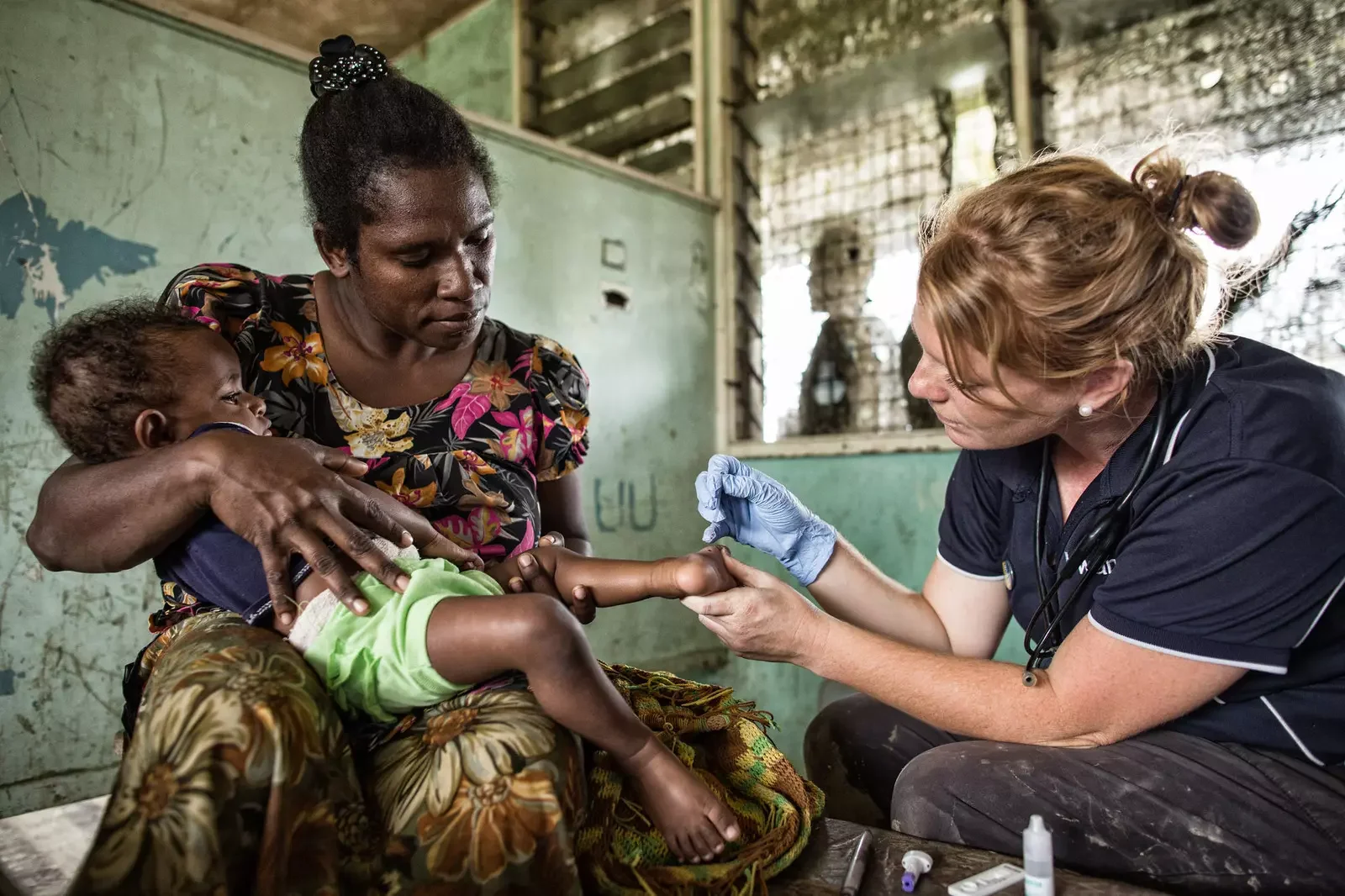
Un trabajador sanitario realiza una prueba preventiva de malaria en un centro de salud de Baimuru, Papúa Nueva Guinea. Allí la malaria sigue siendo endémica, y los modelos climáticos coinciden con la alta prevalencia de variantes inmunitarias heredadas de los denisovanos. Cortesía: YWAM
El mapa evolutivo de la inmunidad
Para entender cómo estas variantes sobrevivieron y se expandieron, hay que mirar al mosaico de entornos que ocuparon los denisovanos:
✅ En Siberia, los análisis paleoclimáticos sitúan la cueva de Denisova en un bosque boreal próximo a la tundra, con inviernos duros que hacían casi imposible la presencia de helmintos intestinales, pero donde proliferaban las garrapatas Ixodes persulcatus, transmisoras de encefalitis vírica y de la bacteria de la enfermedad de Lyme.
✅ En el Tíbet, la cueva de Baishiya se encontraba en un ecosistema frío y seco, más favorable a ciertas formas de leishmaniasis visceral.
✅ En Laos, en cambio, el ambiente monzónico ofrecía un caldo de cultivo para casi todos los agentes patógenos analizados. Esa diversidad de escenarios explica por qué el genoma denisovano acumuló adaptaciones frente a amenazas muy distintas, algunas de las cuales se transmitieron al Homo sapiens y resultaron útiles cuando los seres humanos modernos colonizaron los trópicos.
✅ El caso de Oceanía es especialmente revelador. Allí, donde la huella genética denisovana es más intensa, las condiciones climáticas actuales favorecen la expansión de mosquitos y parásitos similares a los que habrían acosado a los habitantes de la Cobra Cave. En Papúa Nueva Guinea, por ejemplo, la malaria sigue siendo endémica, y los modelos climáticos coinciden con la alta prevalencia de variantes inmunitarias heredadas de los denisovanos. No parece casualidad: las poblaciones que portaban esos genes tenían más posibilidades de sobrevivir y dejar descendencia, de modo que las variantes se consolidaron a lo largo de generaciones. Algo parecido ocurre en Luzón, en Filipinas, donde los análisis también detectan altos niveles de ADN denisovano en paralelo a una elevada exposición histórica a helmintos y malaria.
Una huella genética que no es universal
El estudio no se limita a señalar correlaciones, sino que propone una narrativa evolutiva: cuando los seres humanos modernos llegaron al sudeste asiático, se toparon con un entorno plagado de amenazas invisibles para las que no estaban preparados. Los denisovanos, en cambio, llevaban miles de años enfrentándose a esos mismos patógenos.
👉 El mestizaje les permitió transmitir defensas genéticas ya probadas en el campo de batalla de la coevolución. Así, el ADN denisovano funcionó como una vacuna genética que facilitó al Homo sapiens asentarse en regiones que de otro modo habrían resultado letales.
No obstante, los autores advierten de que la huella genética denisovana no es uniforme ni universal. Muchas de las variantes se perdieron por selección purificadora, especialmente en regiones funcionales del genoma donde podían interferir con el desarrollo normal. Lo que ha llegado hasta nosotros es solo una fracción, y en algunos casos esa fracción conlleva costes.
La relación entre genes arcaicos y enfermedades autoinmunes es un recordatorio de que la evolución no busca la perfección, sino la adaptación inmediata. Además, no todos los grupos humanos recibieron la misma herencia: las poblaciones africanas, que nunca convivieron con denisovanos, carecen de estas variantes, mientras que en Europa predomina más la huella neandertal.
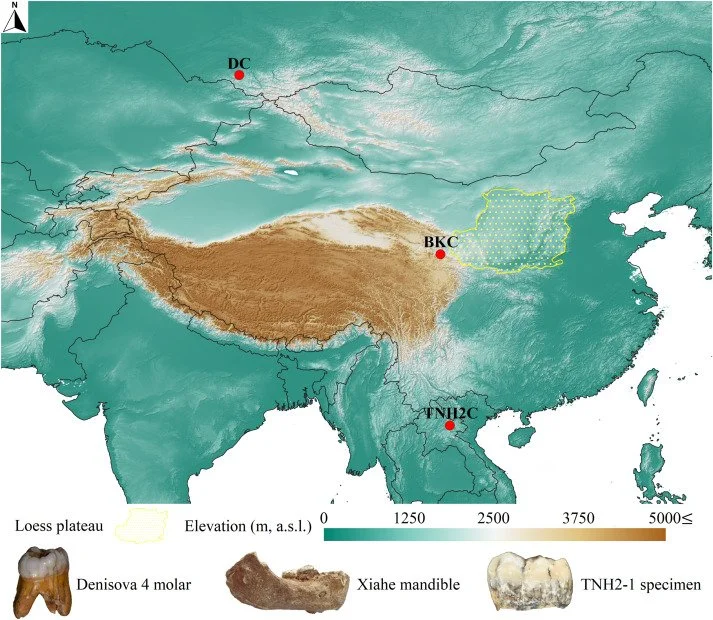
Ubicación geográfica de los yacimientos arqueológicos denisovanos incluidos en el estudio. DC = Cueva Denisova, en las montañas de Altai, sur de Siberia; BKC = Cueva kárstica de Baishiya, en el este de la meseta tibetana; TNH2C = Cueva Tam Ngu Hao 2, en las montañas Annamite. Cortesía: Attila J. Trájer / Science Direct
Implicaciones para la medicina actual
Más allá de las implicaciones médicas, la investigación dibuja un retrato fascinante de la plasticidad de los homínidos. Los denisovanos no fueron una rareza confinada a una cueva siberiana, sino un grupo diverso capaz de sobrevivir en ecosistemas que iban desde las estepas heladas hasta las selvas monzónicas.
Esa versatilidad explica por qué su ADN sigue siendo relevante hoy: su experiencia evolutiva fue más amplia de lo que pensábamos, y al mezclarnos con ellos heredamos un fragmento de esa memoria adaptativa.
El trabajo también abre la puerta a futuras investigaciones biomédicas. Si entendemos qué variantes denisovanas confieren resistencia a enfermedades tropicales, como la malaria y la leishmaniasis, podríamos aprovechar ese conocimiento en la lucha contra epidemias actuales. De hecho, algunos de los genes implicados ya han sido estudiados en relación con la respuesta al coronavirus SARS-CoV-2, y hay evidencias de que la herencia arcaica influyó en la gravedad de la covid-19 en distintos grupos humanos.
👉 No es descabellado por tanto pensar que, en un futuro, la medicina personalizada tenga en cuenta no solo nuestro genoma moderno, sino también el mosaico de fragmentos heredados de otros homínidos.
Un legado que sigue vivo
En definitiva, lo que emerge de este estudio científico es una visión menos lineal y más coral de la evolución humana. No somos descendientes puros de un linaje único, sino herederos de una compleja red de encuentros, cruces y adaptaciones. Los denisovanos, desaparecidos hace decenas de miles de años, siguen presentes en nuestras defensas inmunitarias frente a los parásitos tropicales.
Cada vez que un papú sobrevive a la malaria, o que una población de Filipinas resiste mejor a ciertas infecciones intestinales, resuena la memoria genética de aquellos ancestros olvidados. La historia de nuestra especie, lejos de ser un relato aislado, es un testimonio de mestizaje y de intercambio, donde incluso los grupos que ya no caminan entre nosotros continúan influyendo en nuestro destino. «Los hábitats de los denisovanos moldearon la resistencia a las enfermedades de los humanos modernos», escribe Trajer en su artículo.
Y quizá esa sea la lección más poderosa: que la diversidad genética, incluso a escala evolutiva, es nuestra mejor arma frente a los desafíos del entorno. Los denisovanos desaparecieron, pero dejaron en nosotros un arsenal invisible que todavía hoy salva vidas. Su legado genético nos recuerda que sobrevivir nunca ha sido un esfuerzo individual, sino un proyecto colectivo de la humanidad entera, incluida la de aquellos parientes que solo empezamos a conocer en pleno siglo XXI. ▪️
Fuente: Attila J. Trájer. The role of Denisovan paleohabitats in shaping modern human genetic resistance to viral, bacterial, and parasitic infections. Journal of Human Evolution (2025). DOI: https://doi.org/10.1016/j.jhevol.2025.103746.