Arterias en un chip: los vasos sanguíneos impresos en 3D que podrían descubrir los secretos del ictus
Réplicas microscópicas de arterias humanas, impresas en 3D y cultivadas con células reales, permiten observar cómo nace un ictus en tiempo real. Esta nueva tecnología podría transformar el diagnóstico y la prevención personalizada de los accidentes cerebrovasculares o derrames cerebrales.
Por Enrique Coperías
El investigador Charles Zhao observa de cerca la arteria en chip, una réplica microscópica y funcional de la carótida humana creada mediante impresión 3D. Cortesía: University of Sydney / Fiona Wolf
Cada año, cientos de miles de personas sufren un ictus sin previo aviso. Solo en España afecta a unas 120.000 personas cada año, de las cuales alrededor de 25.000 fallecen. según datos del Ministerio de Salud español.
Muchas de estas obstrucciones cerebrales se originan en la carótida, que es la gran arteria del cuello que abastece de sangre al cerebro, y, sin embargo, la medicina sigue sin saber con precisión por qué unas placas de ateroma acaban rompiéndose y desencadenando un trombo letal y otras no.
A menudo, pacientes catalogados como de bajo riesgo por las guías clínicas actuales terminan padeciendo un accidente cerebrovascular, mientras otros con estrechamientos similares no llegan a enfermar. La geometría de los vasos, la dinámica del flujo sanguíneo, el comportamiento de las células endoteliales y la propia composición de la sangre se entrecruzan en un rompecabezas que la tecnología médica no había conseguido reproducir… hasta ahora.
Una nueva vía inédita para estudiar los derrames cerebrales
Así es, un equipo internacional liderado por la Universidad de Sídney, en Australia, ha logrado imprimir en 3D réplicas microscópicas y totalmente funcionales de la arteria carótida de pacientes reales, a partir de sus angiografías clínicas. Estas arterias en un chip —microdispositivos donde circula sangre humana y se observa la formación de trombos en tiempo real— abren una vía inédita para estudiar el ictus o derrame cerebral de forma personalizada. Y lo hacen con una fidelidad geométrica y biológica nunca antes alcanzada, combinando técnicas avanzadas de imagen, fabricación ultrarrápida, impresión 3D de precisión y modelado computacional del flujo sanguíneo.
🗣️ «No solo estamos imprimiendo vasos sanguíneos: estamos imprimiendo esperanza para millones de personas en riesgo de sufrir un ictus en todo el mundo. Con apoyo y colaboración continuados, queremos hacer que la medicina vascular personalizada sea accesible para cada paciente que la necesite», confiesa Charles Zhao, uno de los ingenieros que han hecho posible el avance.
El resultado es una especie de gemelo vascular, un sistema que replica no solo la forma exacta de los vasos, sino también las fuerzas que actúan sobre la sangre al desplazarse por ellos. Todo ello en una versión reducida treinta veces, pero que mantiene las características esenciales del flujo sanguíneo real.
De un TAC a una arteria viva: cómo se crea el modelo vascular personalizado
El proceso comienza con una angiotomografía computarizada convencional. A partir de esas imágenes, los ingenieros reconstruyen en 3D la anatomía completa de la carótida, incluidas zonas de estenosis, bifurcaciones y ulceraciones.
Este no es un paso trivial: según explican los autores, los sistemas automáticos de reconstrucción suelen pasar por alto detalles clave, sobre todo en áreas donde la placa aterosclerótica presenta cavidades o formas irregulares. Por eso, neurólogos y bioingenieros revisaron a mano cada caso, corrigiendo contornos y verificando continuidad anatómica en cientos de cortes.
Una vez obtenido el modelo digital, entra en juego una de las innovaciones principales del estudio: una técnica ultrarrápida de impresión 3D por procesamiento de luz digital sobre sustrato de vidrio, capaz de reproducir estructuras vasculares de apenas unos cientos de micras. El equipo desarrolló un proceso optimizado que reduce el tiempo de fabricación de más de diez horas a menos de dos, con una tasa de éxito cercana al 100%. En las imágenes microscópicas incluidas en el artículo, puede apreciarse la definición de los moldes, incluso en zonas de curvatura extrema.
🗣️ «Cuando se trata del diagnóstico de infartos e ictus, la rapidez y la precisión son fundamentales —advierte el propio Zhao, cuyo conocimiento en dinámica de fluidos ha sido crucial para la investigación—. Los clínicos suelen tener una ventana de decisión de unas doce horas desde la aparición de los síntomas».
Sobre estos moldes se moldea un chip de PDMS —un polímero transparente muy usado en microfluídica— que se convierte en el canal por donde circulará la sangre. Después, el dispositivo se recubre con fibronectina y se siembra con células endoteliales humanas, que acaban formando una pared biológica completa tras unas horas de incubación.
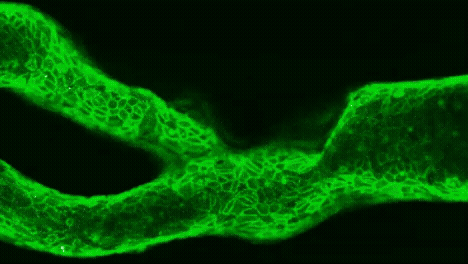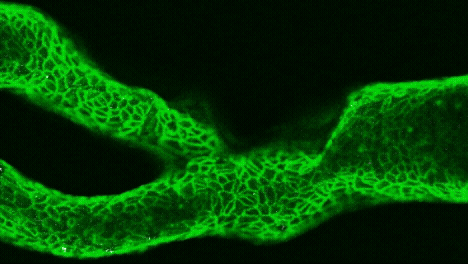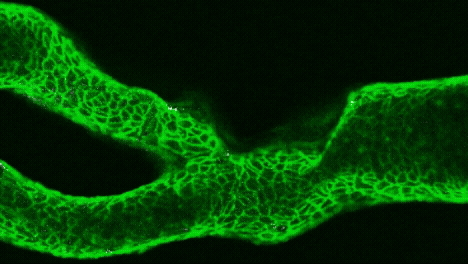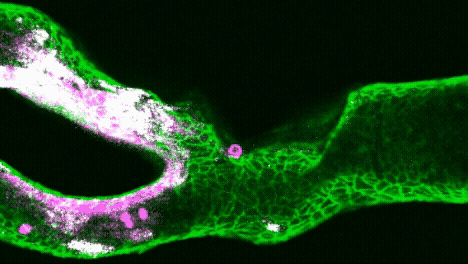
Un trombo, en directo
Vídeo microscópico de un vaso sanguíneo impreso en 3D y recubierto de fibronectina (verde). En uno de los canales se observa la formación de un coágulo (blanco). Cortesía: University of Sydney / Fiona Wolf
Cómo se conservan las propiedades del flujo sanguíneo real en un modelo treinta veces más pequeño
Reducir un vaso real de 6 milímetros a un canal de 200 micras sin perder la dinámica del flujo puede parecer imposible. Pero el grupo solucionó el dilema mediante simulaciones de CFD (dinámica computacional de fluidos) que garantizan que el chip mantenga la misma distribución o velocidad de cizalla (shear rate) que la arteria original del paciente.
Ese parámetro —la fuerza tangencial del flujo sobre las paredes del vaso— resulta crucial en las trombosis, esto es, la formación de un coágulo de sangre o trombo en un vaso sanguíneo que puede obstruir el flujo normal del fluido rojo. Los mapas muestran zonas donde la cizalla supera los 1.000 s⁻¹, consideradas patológicas y fuertemente protrombóticas. Y, sorprendentemente, el chip reproduce esos picos con gran precisión.
Aquí interviene la voz del ingeniero jefe posdoctoral Zihao Wang, que resume así la magnitud del avance: «Esta es la primera iniciativa de bioingeniería de este tipo en Australia, y nuestro trabajo pretende resolver dos brechas cruciales en el diagnóstico y la prevención de las enfermedades cardíacas, sin recurrir a experimentación animal».
🗣️ «Aún hay mucho que no comprendemos sobre el interior de nuestros vasos sanguíneos y sobre lo que desencadena la cascada de eventos que conduce a los coágulos —explica Wang. Y añade—: Hoy no existen plataformas de ensayo a medida que puedan adaptarse a cada paciente. No hay dos pacientes biológicamente iguales: todos ellos presentan diferencias en la estructura de sus vasos y en su sangre, lo que influye en su riesgo de trombosis y en sus opciones de tratamiento».
Gracias a ello, los investigadores pueden perfundir sangre humana y observar adhesión plaquetaria, fibrina y los primeros pasos del ictus isquémico.
Ver nacer un trombo: observación directa de la trombosis en tiempo real
Para explorar la formación global de trombos, el equipo perfundió sangre humana con calcio reintroducido —para activar la coagulación— a través de las arterias en chip. Las imágenes muestran un crecimiento progresivo del coágulo, especialmente en zonas de bifurcación carotídea. El sistema también permite probar anticoagulantes y antitrombóticos en condiciones personalizadas.
A menudo, el desencadenante de la apoplejía es la rotura de una placa. Para imitar ese evento, los investigadores emplearon un sistema de ablación láser de alta precisión que permite reproducir lesiones localizadas en el endotelio.
La investigadora digital Helen Zhao lo describe de la siguiente manera: «Nuestra próxima frontera es integrar la inteligencia artificial (IA) en nuestra plataforma de biofabricación para crear auténticos gemelos digitales que puedan predecir un ictus antes de que ocurra, pasando del tratamiento reactivo a la prevención proactiva. Y añade:
🗣️ «Imagina un futuro en el que podamos tomar la tomografía de un paciente, imprimir rápidamente un modelo de sus vasos sanguíneos, analizar cómo responde su sangre y utilizar la IA para predecir su riesgo de ictus con años de antelación».
El doctor Zihao Wang muestra el dispositivo de vaso sanguíneo impreso en 3D completamente ensamblado. Cortesía: University of Sydney / Fiona Wolf
La geometría vascular sí importa: más allá del porcentaje de estenosis
Los resultados indican que el riesgo real de trombosis no depende solo del porcentaje de estrechamiento, sino de la geometría precisa de la arteria, que incluye:
✅ Ángulos de bifurcación.
✅ Cavidades ulceradas.
✅ Turbulencias microvasculares.
✅ Picos de cizalla local.
Esto explica por qué dos pacientes con estenosis similar pueden tener riesgos opuestos.
¿Hacia una medicina personalizada del ictus?
El avance abre puertas hacia modelos individualizados, gemelos digitales, ensayos de fármacos personalizados y predicción de riesgo de ictus.
«No solo estamos imprimiendo vasos sanguíneos: estamos imprimiendo esperanza para millones de personas en riesgo de ictus en todo el mundo. Con apoyo y colaboración continuados, queremos hacer que la medicina vascular personalizada sea accesible para todo paciente que la necesite», dice e director de Snow Lab, el profesor Arnold Ju.
Por ahora, la arteria en un chip es una herramienta científica poderosa, capaz de revelar fenómenos microscópicos imposibles de observar en el cuerpo humano. Sus implicaciones para el estudio del ictus y la trombosis son profundas. ▪️
Información facilitada por la Universidad de Sídney
Fuente: Yunduo Charles Zhao, Zihao Wang et al. Rapid Glass-Substrate Digital Light 3D Printing Enables Anatomically Accurate Stroke Patient-Specific Carotid Artery-on-Chips for Personalized Thrombosis Investigation. Advanced Materials (2025). DOI: https://doi.org/10.1002/adma.202508890