Descubren que el tejido que rodea al tumor puede activar la metástasis del cáncer de mama
Un estudio revela que el entorno físico del tumor no es un mero espectador, sino un actor clave en la expansión de las células malignas por el organismo. La rigidez del tejido puede desatar los mecanismos que permiten al cáncer de mama hacer metástasis.
Por Enrique Coperías, periodista científico
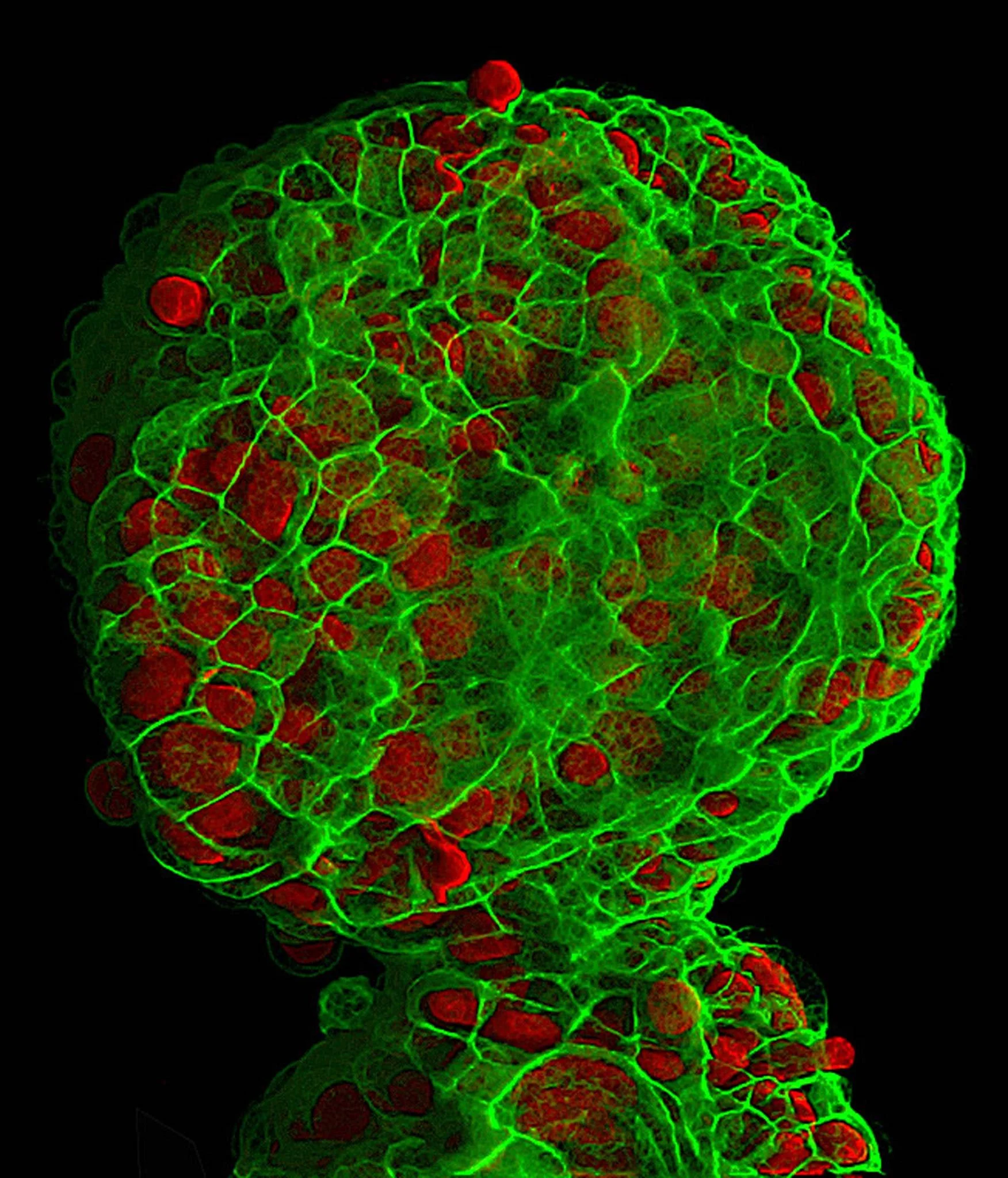
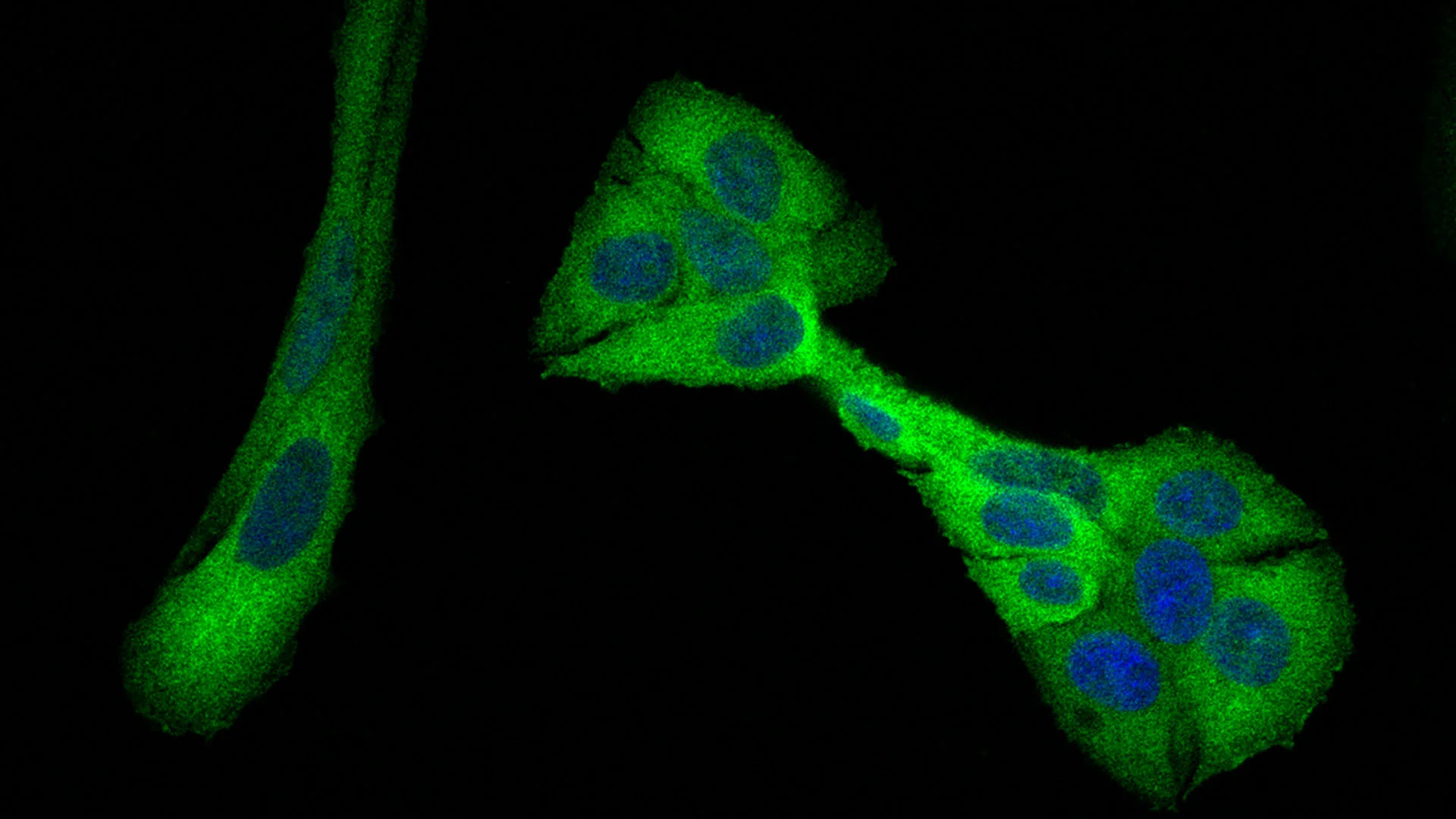
Imagen tridimensional de células de cáncer de mama cultivadas en laboratorio: en verde, la estructura celular; en rojo, núcleos o células en proliferación. Este modelo reproduce el entorno del tumor y ha permitido identificar cómo la rigidez del tejido que lo rodea puede activar la metástasis al desactivar el papel protector de la proteína TYK2. Cortesía: Dr. Jônatas Bussador do Amaral & Dr. Gláucia Maria Machado Santelli / University of São Paulo
¿Por qué es importante la metástasis en el cáncer de mama?
La metástasis sigue siendo el gran enigma —y el mayor verdugo— del cáncer. En el caso del cáncer de mama, no es el tumor primario el que suele matar, sino su capacidad para extenderse a otros órganos; por lo general, a los huesos, los pulmones, el cerebro y el hígado. Entre un 5 y un 6% de los cánceres de mama presentan metástasis en el momento del diagnóstico.
Ahora, un equipo de oncólogos de la Universidad de California en San Diego (Estados Unidos) ha identificado un mecanismo inesperado que ayuda a explicar cómo y cuándo se activa ese proceso letal. Y la clave no está solo en las células tumorales, sino en algo mucho más sutil: la rigidez del tejido que las rodea.
El hallazgo, descrito en un estudio publicado en la revista Nature Communications, apunta a una proteína poco explorada en este contexto como un guardián molecular que frena la metástasis en condiciones normales: la TYK2. Pero cuando ese sistema falla —o se inhibe farmacológicamente—, las células cancerosas parecen encontrar vía libre para invadir el organismo.
El descubrimiento: el entorno físico del tumor influye en su agresividad
Durante años, la investigación oncológica se ha centrado casi exclusivamente en las mutaciones genéticas de las células tumorales. Sin embargo, en la última década ha emergido con fuerza otro protagonista: el microambiente tumoral. Es decir, el tejido que rodea al tumor, que está compuesto por proteínas, fibras y señales físicas.
Entre esas características, la rigidez del tejido, o sea, cómo es de duro o blando, se ha convertido en un factor clave. Tanto es así que los tumores más inflexibles, ricos en fibras y cicatrización, se asocian con peor pronóstico y mayor capacidad de diseminación.
El nuevo estudio da un paso más en esta dirección: no solo confirma que la rigidez importa, sino que revela cómo las células sienten esa firmeza y la traducen en decisiones biológicas.
🗣️ «Este estudio nos desvela cómo la rigidez de la matriz extracelular regula la metástasis del cáncer de mama a través de TYK2 y aporta nuevos conocimientos sobre cómo las señales físicas del microambiente tumoral controlan la progresión del cáncer», explica Zhimin Hu, investigador principal del trabajo e investigador en el Departamento de Farmacología del Moores Cancer Center en la UCSan Diego.
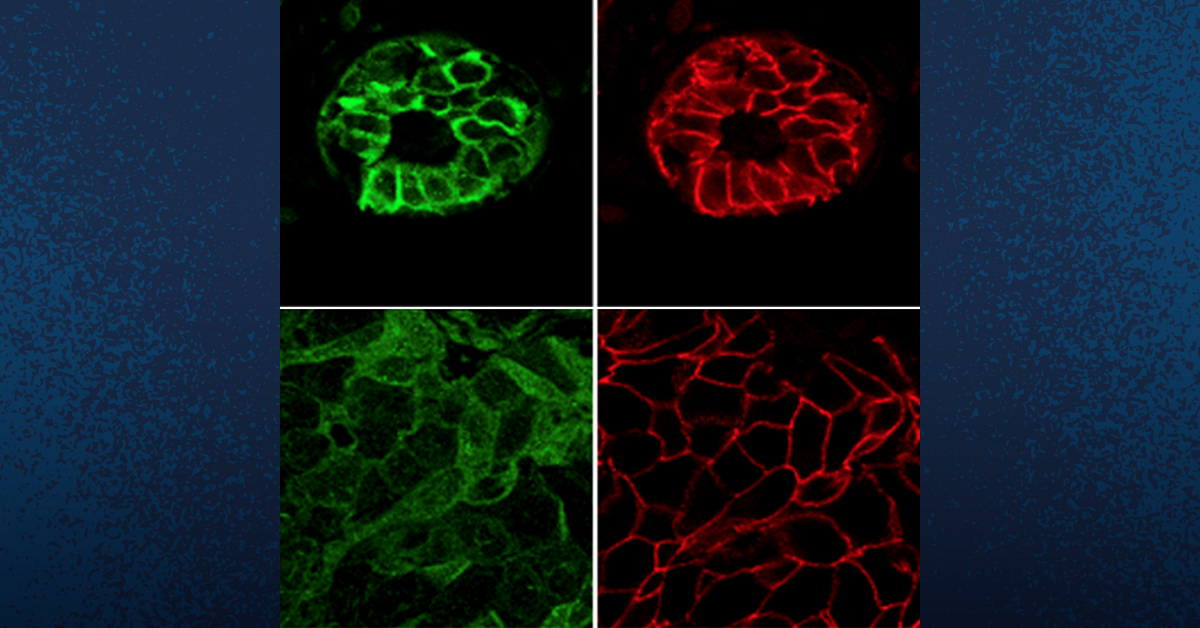
En tejidos sanos (paneles superiores), TYK2 (verde) se localiza en la membrana celular y colocaliza con E-cadherina (rojo), clave para la adhesión y la integridad del tejido. En tumores (paneles inferiores), TYK2 se dispersa dentro de la célula y pierde esa colocalización, facilitando la diseminación de las células cancerosas. Cortesía: UC San Diego Health Sciences
Qué es la TYK2 y cuál es su papel en el cáncer de mama
La proteína tirosina quinasa 2 o TYK2 pertenece a una familia proteica conocida por su papel en la respuesta inmunitaria. Hasta ahora, su función se había estudiado casi exclusivamente en células del sistema de defensa. Pero este trabajo muestra que también actúa en células del tejido mamario con una función crucial: evitar que adopten un comportamiento invasivo.
En condiciones normales —cuando el tejido es blando, como en una mama sana— la TYK2 se sitúa en la membrana celular y mantiene a raya un programa biológico llamado transición epitelio-mesénquima (EMT). Este programa permite a las células perder su cohesión y adquirir movilidad, un paso esencial para la metástasis.
Sin embargo, cuando los investigadores bloquearon a la TYK2 —ya fuera genéticamente o mediante fármacos— observaron algo llamativo: incluso en los tejidos blandos, las células comenzaban a comportarse como si estuvieran en un entorno tumoral agresivo. Invadían, se dispersaban y activaban ese programa metastásico.
Cómo funciona el mecanismo: del tejido blando al tumor invasivo
El mecanismo descubierto es, en esencia, un sistema de traducción entre el mundo de la física y el de la biología. Así es, las células no solo responden a señales químicas, sino también a fuerzas mecánicas:
✅ En tejidos blandos, la TYK2 permanece activo y localizado en la membrana celular, donde bloquea una cadena de eventos que llevaría a la metástasis.
✅ Pero cuando el tejido se vuelve rígido, como ocurre en algunos tumores, la TYK2 cambia de posición dentro de la célula, se inactiva y deja de ejercer su función protectora.
Ese cambio permite que otra proteína clave, la TWIST1, entre en el núcleo y active genes asociados con la invasión celular. En otras palabras, el endurecimiento del tejido actúa como un interruptor que libera el potencial metastásico.
Hay que señalar que la TWIST1 es un factor de transcripción que regula la transición epitelio-mesénquima (EMT), un proceso por el cual las células pierden su adhesión y adquieren capacidad de movimiento. En condiciones normales, participa en el desarrollo embrionario, pero en el cáncer su activación favorece que las células tumorales se vuelvan más invasivas y puedan diseminarse a otros órganos. O sea, que la TWIST1 convierte células quietas en células capaces de migrar y diseminarse.
El viaje hasta el pulmón
Los investigadores no se quedaron en experimentos celulares. También probaron sus hipótesis en modelos animales y en organoides derivados de pacientes, pequeñas estructuras tridimensionales que imitan a los tumores reales.
El resultado fue consistente: la inhibición de la TYK2 no aumentaba el tamaño del tumor primario, pero sí disparaba la aparición de metástasis, especialmente en los pulmones.
Este dato es especialmente relevante, porque refuerza una idea cada vez más aceptada en oncología: el crecimiento del tumor y su capacidad de diseminarse son procesos distintos, gobernados por mecanismos diferentes.
Implicaciones clínicas: riesgos de los inhibidores de la TYK2
Quizá la parte más inquietante del nuevo trabajo tiene que ver con los tratamientos ya existentes. En los últimos años, se han desarrollado fármacos que inhiben la TYK2 para tratar enfermedades autoinmunes como la psoriasis.
Estos medicamentos, como el deucravacitinib, han mostrado gran eficacia clínica. Pero los nuevos datos sugieren que podrían tener un efecto no deseado: favorecer la metástasis en ciertos contextos, especialmente en pacientes con lesiones tumorales no diagnosticadas.
Los autores no plantean una alarma inmediata, pero sí una advertencia clara: podría ser necesario reforzar el cribado de cáncer de mama en pacientes que reciben este tipo de terapias.
🗣️ «Nuestros hallazgos tienen importantes implicaciones para el uso clínico de los inhibidores de TYK2 y subrayan la importancia de tener en cuenta el microambiente mecánico en la terapia contra el cáncer», señala Jing Yang, autora senior del estudio en el Moores Cancer Center.
Más allá de la genética
El estudio encaja en una transformación más amplia en la investigación del cáncer. Durante décadas, la narrativa dominante ha sido genética: mutaciones, oncogenes, supresores tumorales... Pero cada vez hay más evidencia de que el cáncer es también un fenómeno físico.
Las células no viven en el vacío. Están inmersas en un entorno que las empuja, las comprime, las estira. Y esas fuerzas pueden ser tan determinantes como cualquier mutación.
En este caso, la rigidez del tejido no solo acompaña al tumor, sino que participa activamente en su evolución.
Una nueva ventana terapéutica contra el cáncer de mama
Comprender estos mecanismos abre nuevas posibilidades en la lucha contra el cáncer mamario, que solo en España afecta cada año a más 36.000 mujeres y causa unos 6.000 fallecimientos. Si la rigidez del tejido y la localización de proteínas como la TYK2 determinan el comportamiento tumoral, entonces podrían convertirse en dianas terapéuticas.
En lugar de atacar directamente a las células cancerosas, una estrategia podría consistir en modificar su entorno o restaurar los mecanismos que mantienen su comportamiento normal.
No es una idea nueva, pero este trabajo aporta una pieza clave al puzle: identifica un intermediario molecular concreto que conecta el mundo físico con el biológico.
El futuro pasa por entender el entorno del tumor
Aún quedan muchas preguntas abiertas, como estas que destaca Hu:
✅ ¿Cómo las células detectan con exactitud la rigidez del tejido?
✅ ¿Por qué algunos tumores son más sensibles que otros?
✅ ¿Se puede revertir este proceso?
Pero el mensaje principal es claro: para entender la metástasis, no basta con mirar dentro de la célula. Hay que mirar también fuera.
Porque, como muestra este estudio, a veces el destino de un cáncer no depende solo de lo que es, sino de dónde está y de cómo se siente.▪️(1-abril-2026)
PREGUNTAS&RESPUESTAS: Cáncer de Mama y Metástasis
🩺 ¿Qué es la metástasis en el cáncer de mama?
Es la diseminación de células cancerosas desde la mama hacia otros órganos como pulmones, hígado o huesos.
🩺 ¿Qué función tiene la proteína TYK2?
Actúa como un supresor de metástasis, evitando que las células cancerosas se vuelvan invasivas en condiciones normales.
🩺 ¿Por qué es importante la rigidez del tejido?
Porque determina si las células activan mecanismos de invasión y propagación del cáncer.
🩺 ¿Los fármacos inhibidores de TYK2 son peligrosos?
Podrían aumentar el riesgo de metástasis en ciertos contextos, por lo que se recomienda más investigación y vigilancia clínica.
Fuente: Hu, Z., Majeski, H.E., Mestre-Farrera, A. et al.Extracellular matrix rigidity controls breast cancer metastasis via TYK2-mediated mechanotransduction.Nature Communications (2026). DOI: https://doi.org/10.1038/s41467-026-70518-9