El gen del anfibio que podría abrir la puerta a regenerar extremidades humanas
Un mecanismo genético compartido por ajolotes, peces y mamíferos desvela que la regeneración de extremidades no es una excepción evolutiva, sino una capacidad latente. Un nuevo estudio apunta a que la terapia génica podría activar ese potencial en los seres humanos y transformar la medicina regenerativa.
Por Enrique Coperías, periodista científico
Un ajolote en el Laboratorio de Regeneración del biólogo Josh Currie (Universidad de Wake Forest), una especie clave para estudiar los genes que permiten regenerar extremidades y que podrían inspirar futuras terapias en humanos. Cortesía: Wake Forest University
Un hallazgo clave en medicina regenerativa
Un gen compartido por especies tan dispares como el ajolote (Ambystoma mexicanum), el pez cebra (Danio rerio) o el ratón podría abrir una vía inesperada hacia uno de los grandes retos de la medicina regenerativa: la capacidad de volver a hacer crecer extremidades humanas.
Así lo sugiere una investigación internacional en la que participa el biólogo de la Universidad de Wake Forest Josh Currie y cuyos resultados han sido publicados en la revista Proceedings of the National Academy of Sciences (PNAS).
El estudio parte de una pregunta que lleva décadas intrigando a la biología: ¿por qué algunos animales pueden regenerar partes completas del cuerpo y otros, como los seres humanos, apenas conservan esa capacidad?
¿Por qué es importante este descubrimiento?
Cada año, se producen en el mundo más de un millón de amputaciones, según el informe estadístico anual Global Burden of Diseases. Las mutilaciones se deben principalmente a:
✅ Enfermedades vasculares.
✅ Traumatismos.
✅ Cánceres.
✅ Infecciones.
Y se espera que la cifra aumente con el envejecimiento de la población y el incremento de la diabetes. Esta puede dañar los vasos sanguíneos y los nervios, especialmente en los pies y las piernas, lo que reduce la circulación y la sensibilidad. Esto favorece la aparición de heridas que no cicatrizan, infecciones graves y, en casos avanzados, hace necesaria la amputación de un miembro o parte de él para evitar complicaciones mayores.
Ante ese escenario, los científicos buscan alternativas que vayan más allá de las prótesis, las cirugías reconstructivas y las rehabilitaciones, y permitan recuperar no solo la forma, sino también la función de una extremidad.
El cometido de los genes SP6 y SP8
La clave para que el milagro de la regeneración de nuestras extremidades sea posible podría residir, según este trabajo, en un conjunto de genes conocidos como genes SP, en particular el SP6 y el SP8.
🗣️ «Esta importante investigación reunió a tres laboratorios, que trabajaron con tres organismos distintos para comparar la regeneración —afirma Currie, cuyo laboratorio está especializado en el estudio del ajolote, una especie de anfibio originaria de México de la familia de los ambistomátidos y relacionada con la salamandra tigre. Y añade—: [El estudio] nos demostró que existen programas genéticos universales y comunes que impulsan la regeneración en tipos de organismos tan diferentes como los ajolotes, los peces cebra y los ratones».
La elección de estas tres especies no es fortuita:
1️⃣ El ajolote es capaz de regenerar extremidades completas, así como partes del corazón, el cerebro o la médula espinal.
2️⃣ El pez cebra, por su parte, puede reconstruir rápidamente sus aletas caudales y también regenerar órganos internos.
3️⃣ Los ratones representan el modelo mamífero: aunque su capacidad es mucho más limitada, pueden volver a crecer las puntas de los dedos, un fenómeno que también ocurre en los seres humanos si la lesión conserva el lecho ungueal, la piel debajo de la uña.
A partir de esa comparación, los científicos observaron que, en los tres casos, la epidermis regenerativa —la capa de piel que cubre la herida— activa los genes SP6 y SP8. El siguiente paso fue comprobar su función. Mediante la tecnología de edición genética CRISPR o cortapega genético, el equipo eliminó el gen SP8 en ajolotes. El resultado fue contundente: sin él, estos anfibios eran incapaces de regenerar correctamente los huesos de las extremidades. Algo similar ocurrió en ratones a los que se les suprimieron SP6 y SP8.
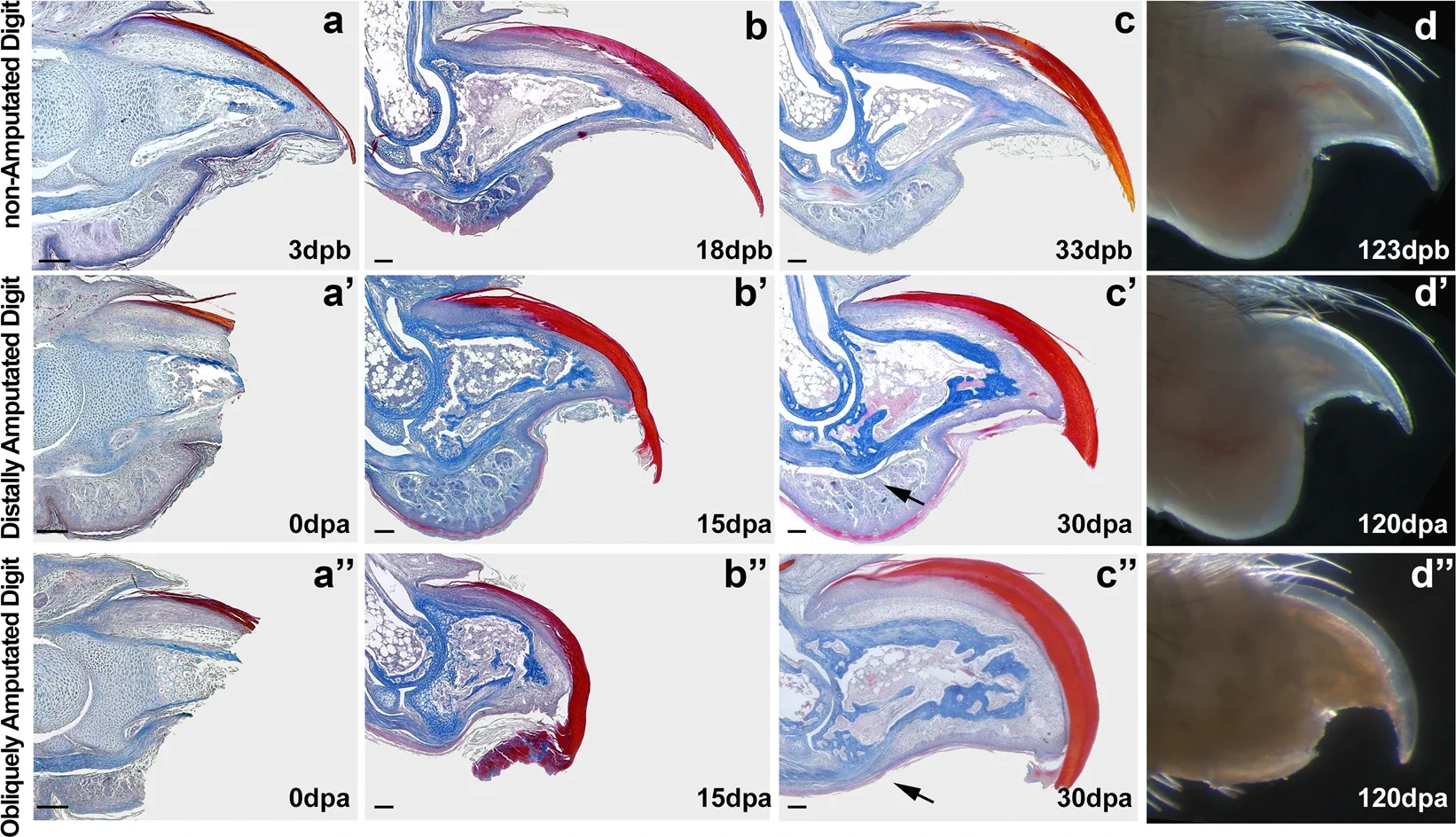
Secciones histológicas de puntas de dedos de ratón que comparan el desarrollo normal y la regeneración tras una amputación. Las imágenes muestran la evolución temporal del tejido en controles no amputados y en dedos amputados (distal y oblicuamente), lo que evidencia distintos grados de regeneración ósea y tisular; las flechas señalan la presencia o ausencia de la almohadilla grasa. Cortesía: Sensiate, L. A., Marques-Souza, H.
Cómo funciona la nueva terapia génica
Con ese conocimiento en la mano, Currie y sus colegas dieron un paso más hacia la aplicación terapéutica. El laboratorio de David A. Brown, cirujano plástico en la Universidad Duke, en Estados Unidos, utilizó un potenciador de regeneración tisular procedente del pez cebra para diseñar una terapia génica basada en vectores virales.
Esta estrategia permitió introducir en los tejidos lesionados una molécula llamada factor de crecimiento de fibroblastos 8 (FGF8), normalmente activada por el gen SP8, que favorece el crecimiento óseo.
En los experimentos con ratones, esta terapia génica logró compensar parcialmente la ausencia de los genes SP y acelerar la regeneración de las puntas de los dedos. Aunque todavía lejos de la complejidad de una extremidad completa, los resultados apuntan a una prueba de concepto prometedora.
Del embrión para los adultos
«Podemos utilizar esto como una especie de prueba de principio de que podríamos ser capaces de desarrollar terapias que sustituyan a este tipo de regeneración de la epidermis en la regeneración de tejidos en seres humanos», explica Currie.
El estudio también aporta una visión más amplia sobre los mecanismos biológicos implicados. En palabras de este biólogo, él y sus colegas han identificado un programa transcripcional conservado en la epidermis que coordina la regeneración y que incluye respuestas inflamatorias específicas, como la activación de los osteoclastos —células que reabsorben y remodelan hueso— mediada por la interleucina-17, una citoquina proinflamatoria.
Este entramado conecta procesos del desarrollo embrionario con la regeneración en individuos adultos, una relación que hasta ahora no estaba del todo clara.
Aleta caudal de pez cebra en proceso de regeneración, donde el nuevo hueso (en verde) crece guiado por señales moleculares (en rosa), un modelo clave para entender cómo algunos vertebrados pueden reparar tejidos a lo largo de toda su vida. Cortesía: Sushant Bangru
Implicaciones para la medicina humana
Pese al entusiasmo, los investigadores subrayan que el camino hacia una terapia aplicable en humanos será largo.
✅ «Los científicos están explorando numerosas soluciones para la sustitución de extremidades, entre las que se incluyen los andamios bioingenierizados y las terapias con células madre —recuerda Currie. Y añade—: El enfoque de terapia génica de este estudio es una nueva vía que puede complementar y, en teoría, potenciar lo que sin duda será una solución multidisciplinar para regenerar algún día las extremidades humanas».
Más allá de los resultados concretos, el trabajo destaca también por su enfoque colaborativo, poco habitual en un campo donde los modelos animales suelen estudiarse por separado.
«Muchas veces los científicos trabajan en compartimentos estancos: solo en ajolotes, o solo en ratón, o solo en peces —reflexiona Currie. Y concluy—: Una característica realmente destacada de esta investigación es que trabajamos a través de todos estos organismos. Eso es muy potente y es algo que espero que veamos más en este campo».
La idea de volver a hacer crecer un brazo o una pierna sigue siendo, por ahora, territorio de la ciencia ficción. Pero estudios como este sugieren que la respuesta podría no estar en inventar algo completamente nuevo, sino en aprender a activar, o imitar, programas genéticos de regeneración que la evolución ya ha perfeccionado en otras especies.▪️(18-abril-2026)
PREGUNTAS&RESPUESTAS: Extremidades y Regeneración
💪 ¿Es posible regenerar extremidades humanas hoy en día?
No. Actualmente no existe ninguna técnica capaz de regenerar extremidades completas en seres humanos.
💪 ¿Qué aporta este descubrimiento?
Identifica genes clave y demuestra que se pueden activar procesos regenerativos mediante terapia génica.
💪 ¿Cuánto falta para aplicarlo en pacientes?
Aún se necesitan años de investigación y ensayos clínicos.
💪 ¿Qué es la FGF8?
Es una proteína que estimula el crecimiento de tejidos y está implicada en procesos de desarrollo y regeneración.
💪 ¿Por qué se estudian animales como el ajolote?
Porque poseen una capacidad regenerativa natural que permite identificar mecanismos aplicables a otras especies.
Información facilitada por la Wake Forest University
Fuente: D. A. Brown et al. Enhancer-directed gene delivery for digit regeneration based on conserved epidermal factors. PNAS (2026). DOI: https://doi.org/10.1073/pnas.2532804123