Espermatozoides convertidos en microrrobots magnéticos: la revolución de la fertilidad y la medicina reproductiva
De invisibles a controlables: científicos han transformado espermatozoides en microrrobots magnéticos capaces de moverse bajo campos externos y ser vistos en rayos X, abriendo así un nuevo horizonte en fertilidad y terapias ginecológicas.
Por Enrique Coperías
Ilustración conceptual de espermatozoides recubiertos con nanopartículas magnéticas, visibles bajo rayos X y guiados por campos magnéticos. Una innovación que abre la puerta a diagnósticos de infertilidad y terapias dirigidas en medicina reproductiva. Imagen generada con DALL-E
La fertilidad humana sigue siendo, en pleno siglo XXI, un terreno sembrado de incógnitas. Se estima que entre un 10% y un 15% de las parejas en edad reproductiva experimentan problemas para concebir, y en casi la mitad de los casos la causa sigue siendo un misterio.
Uno de los grandes obstáculos para avanzar en los diagnósticos y los tratamientos es, paradójicamente, nuestra limitada capacidad para observar lo que ocurre dentro del aparato reproductor femenino en tiempo real. ¿Cómo se desplazan los espermatozoides? ¿Dónde se almacenan? ¿Qué interacciones químicas y físicas experimentan en su camino hacia el óvulo?
Responder a estas preguntas no solo aclararía las raíces de muchas infertilidades inexplicables, sino que abriría la puerta a nuevas técnicas de reproducción asistida y terapias dirigidas.
Espermatozoides recubiertos con nanopartículas magnéticas
Un grupo internacional de investigadores de la Universidad de Twente (Países Bajos), la Universidad de Waterloo (Canadá) y el Radboud University Medical Center (Países Bajos) ha presentado un avance sorprendente: espermatozoides recubiertos con diminutas nanopartículas magnéticas capaces de ser guiados desde el exterior mediante campos magnéticos y, además, visibles en tiempo real gracias a rayos X.
El estudio, publicado en la revista npj Robotics, supone la primera demostración de microrobots espermáticos controlables y rastreables simultáneamente en un modelo anatómico 3D del aparato reproductor femenino.
Más allá de lo llamativo de la imagen —espermatozoides convertidos en nanorrobots—, este trabajo abre un horizonte con aplicaciones que van desde la mejora de técnicas de fertilización hasta tratamientos innovadores contra el cáncer ginecológico.
Tras los escurridizos espermatozoides
Hasta ahora, las técnicas para observar espermatozoides en movimiento dentro del cuerpo eran limitadas. Se han probado métodos ópticos, como la microscopía de fluorescencia y la tomografía de coherencia óptica, pero su alcance es reducido: apenas permiten penetrar unos pocos milímetros en el tejido y, en ocasiones, requieren intervenciones invasivas en animales de laboratorio. No existe una técnica sencilla y no invasiva para seguir a estas células en su periplo natural.
«Hasta ahora, visualizar esperma dentro del cuerpo era casi imposible», resume Islam Khalil, investigador del TechMed Centre de la Universidad de Twente y autor principal del trabajo. La dificultad radica en que los espermatozoides son células minúsculas, de baja densidad y casi transparentes a la radiación, por lo que pasan inadvertidos a técnicas como los rayos X o la ecografía convencional.
La robótica microscópica llevaba años tanteando este terreno. La idea de usar células vivas combinadas con materiales sintéticos para crear microrobots biohíbridos ya había mostrado resultados prometedores. Estos nuevos microrrobots pueden moverse de forma inalámbrica, transportar pequeñas cargas, como fármacos, y, al estar basados en células, presentan buena compatibilidad biológica. Pero faltaba un paso crucial: conseguir que fueran detectables y controlables de manera simultánea dentro de un entorno realista.
¿Qué son los microrrobots espermáticos?
La innovación de este trabajo consiste en cubrir espermatozoides con nanopartículas de óxido de hierro. Gracias a la carga eléctrica de la superficie celular, las partículas se autoensamblan alrededor de la membrana, creando estructuras flexibles y magnéticas. Al agruparse varios de estos espermatozoides recubiertos se forman clústeres que responden a campos magnéticos externos.
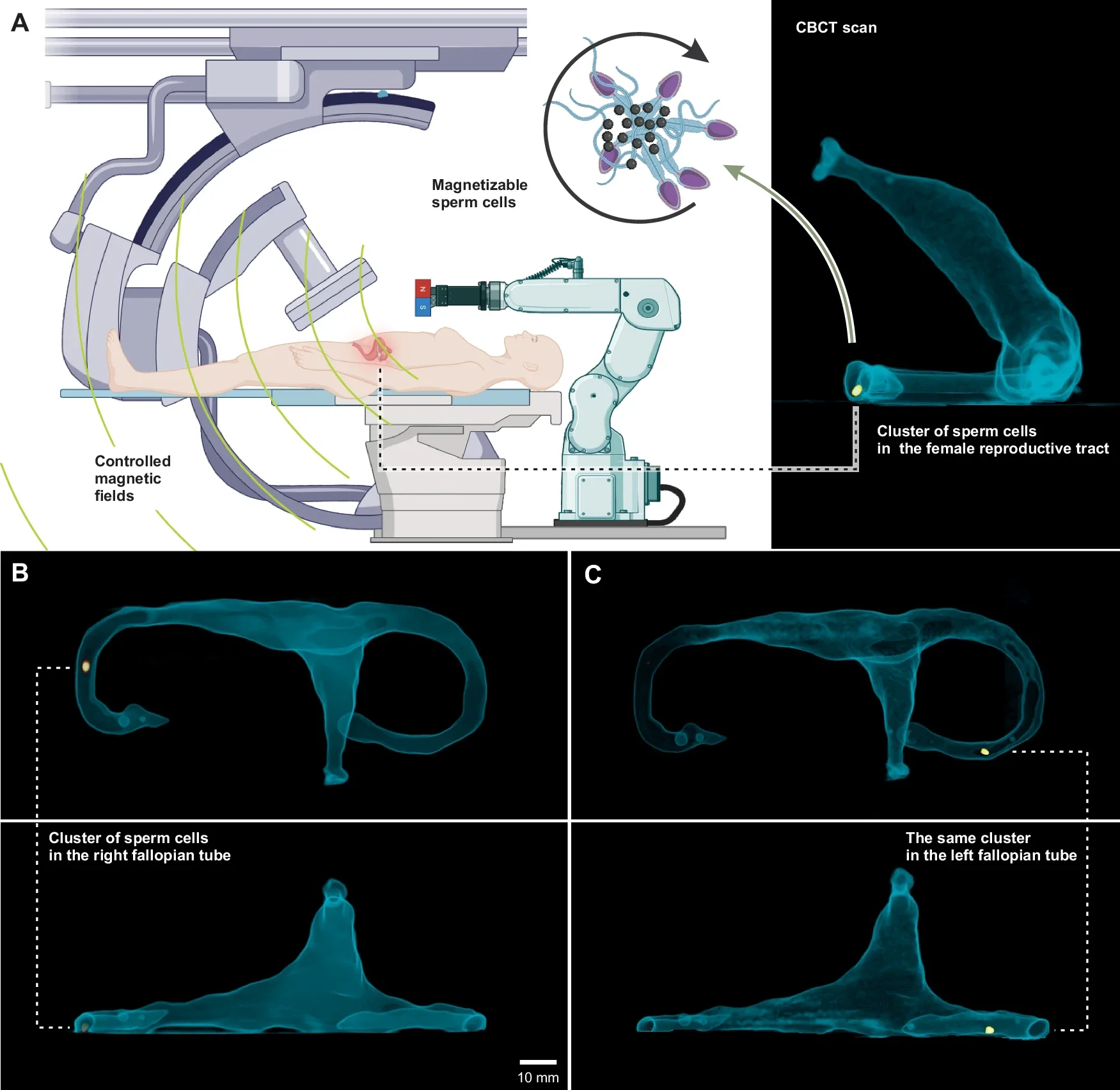
El equipo usó un sistema de imanes rotatorios que inducen un movimiento de rodadura de los grupos de espermatozoides, lo que permite desplazarlos con bastante precisión. Al mismo tiempo, estos clústeres son visibles mediante fluoroscopia de rayos X y ultrasonidos, dos técnicas clínicas habituales. Por primera vez, se logró la hazaña de moverlos dentro de un modelo 3D del aparato reproductor femenino impreso en resina y, al mismo tiempo, seguir su recorrido en directo en una pantalla.
El efecto es tan realista que los investigadores pudieron dirigir los microrrobots desde el cuello uterino hasta las trompas de Falopio en menos de un minuto, controlando giros, bifurcaciones y hasta ascensos contra la gravedad.
Un laboratorio dentro del útero
Para validar la técnica, el equipo creó un modelo anatómico a tamaño real del aparato reproductor femenino, basado en imágenes médicas reales. Este duplicado impreso en 3D se llenó con solución salina para simular el entorno fisiológico.
Bajo fluoroscopia, los clústeres de espermatozoides magnéticos eran claramente visibles como manchas móviles que los investigadores guiaban con un brazo robótico equipado con imanes.
Los experimentos demostraron que los microrrobots podían recorrer desde el cuello uterino hasta los extremos distales de las trompas de Falopio en menos de 50 segundos, navegando con precisión sorprendente. La velocidad, cercana a unos pocos milímetros por segundo, es suficiente para emular el tiempo real de procesos reproductivos.
Microrobots biohíbridos basados en espermatozoides, guiados con campos magnéticos externos débiles y de baja frecuencia, y localizados mediante fluoroscopia de rayos X para posibles tratamientos mínimamente invasivos en el aparato reproductor femenino. Esquema (izq.) y tomografía CBCT (der.) muestran cúmulos de espermatozoides recubiertos con nanopartículas en trompas de Falopio de un modelo anatómico. Estos microrobots biohíbridos pueden guiarse con campos magnéticos y visualizarse con rayos X para tratamientos mínimamente invasivos en salud reproductiva. Cortesía: Magdanz, V. et al / Nature
Una tecnología con vocación médica
Los autores destacan varias ventajas de este nuevo enfoque biotecnológico:
✅ Mayor control que con espermatozoides vivos: al estar recubiertos de nanopartículas y actuar como plantillas, los microrrobots no dependen del movimiento autónomo de la célula viva. Se pueden dirigir con total control de dirección y velocidad.
✅ Visibilidad clínica: a diferencia de espermatozoides individuales, invisibles para técnicas de imagen, los clústeres recubiertos aparecen claramente en rayos X y ecografías.
✅ Compatibilidad biológica: los ensayos de toxicidad celular en células uterinas mostraron que los recubrimientos de hierro no dañaban significativamente los tejidos, incluso tras 72 horas de exposición.
✅ Capacidad de carga: cada espermatozoide conserva su membrana, que actúa como una pequeña cápsula de transporte capaz de llevar moléculas. En estudios previos, se logró cargar estos clústeres con un fármaco anticancerígeno, demostrando que podrían servir como sistemas de liberación dirigida de medicamentos dentro del aparato reproductor.
«Estamos transformando el propio sistema de transporte celular de la naturaleza en microrobots programables», explica Khalil. La idea no es solo elegante desde el punto de vista científico: podría convertirse en una herramienta poderosa para la administración precisa de fármacos en zonas de difícil acceso, como el endometrio y las trompas de Falopio.
👉 Enfermedades como el cáncer uterino, la endometriosis y los fibromas uterinos carecen hoy de tratamientos dirigidos que actúen directamente en el tejido afectado.
Imagen de microscopía electrónica de espermatozoides convertidos en nanorrobots magnéticos. Cortesía: TechMed Centre
Qué ocurre en la fecundación
Además de su potencial terapéutico, esta tecnología abre una ventana inédita a uno de los mayores misterios de la biología: qué ocurre exactamente durante la fecundación en el interior del cuerpo femenino.
Poder seguir el trayecto de los espermatozoides de manera no invasiva permitirá, sin duda alguna, estudiar con más detalle cómo se mueven, qué obstáculos encuentran y por qué en algunos casos no llegan a fecundar al óvulo.
Los investigadores confían en que esto ayude a desentrañar muchos casos de infertilidad inexplicable y, en paralelo, permita perfeccionar técnicas como la fecundación in vitro (FIV), al comprender mejor las condiciones óptimas de transporte de los gametos.
«La posibilidad de rastrear el movimiento del esperma dentro del aparato reproductor abre la puerta a mejorar tanto el diagnóstico de la infertilidad como los tratamientos», señalan los autores.
Equilibrio entre eficacia y toxicidad
Uno de los grandes dilemas de la nanomedicina es la denominada triple balanza: cuanto más material magnético se añade, mejor es la visibilidad y la capacidad de control, pero también aumenta el riesgo de toxicidad. Los investigadores probaron distintas concentraciones de nanopartículas (1, 2 y 3 mg/mL) y observaron que, dentro de ese rango, la viabilidad celular se mantenía estable.
Curiosamente, los propios espermatozoides limpios, o sea, sin nanopartículas, resultaron más dañinos para las células uterinas que los híbridos, posiblemente por residuos del proceso de conservación del semen.
Otro hallazgo importante es que la velocidad de movimiento de los clústeres no depende tanto de la cantidad de nanopartículas como de su tamaño y forma. Los más grandes tienden a rodar más deprisa, pero también son más frágiles y tienden a fragmentarse. Aun así, incluso cuando se rompían en fragmentos más pequeños, el campo magnético conseguía mantenerlos cohesionados y avanzando hechos un piña.
¿Hacia dónde apunta esta tecnología?
Las aplicaciones potenciales son múltiples. Estas son alguna de las que proponen Khalil y su equipo:
✅ Diagnóstico de infertilidad: poder seguir el trayecto de espermatozoides en tiempo real permitiría identificar obstrucciones en las trompas, alteraciones en el entorno uterino o patrones de movilidad anómalos.
✅ Reproducción asistida de nueva generación: los microrobots podrían transportar gametos o embriones iniciales hasta lugares específicos, aumentando las probabilidades de éxito en casos complejos.
✅ Terapia dirigida contra enfermedades ginecológicas: endometriosis, fibromas uterinos e incluso cáncer de útero y ovario podrían beneficiarse de una liberación localizada de fármacos, y evitando los efectos secundarios de tratamientos sistémicos.
✅ Investigación básica en fertilidad: comprender con mayor detalle cómo interactúan los espermatozoides con el microambiente uterino puede arrojar luz sobre procesos biológicos aún poco explorados.
«Este avance podría abrir nuevas puertas en medicina reproductiva, en la administración de fármacos y en el diagnóstico de la infertilidad», resume Khalil en un comunicado del TechMed Centre.
Un paso más hacia la medicina del futuro
Aunque los resultados son prometedores, aún quedan desafíos importantes antes de pensar en ensayos clínicos. Uno de ellos es la fragmentación de los clústeres, que podría complicar el control en entornos más viscosos, como los fluidos reales del aparato reproductor. También será necesario estudiar cómo se comportan en tejidos vivos, con pliegues, secreciones y corrientes naturales.
Otro frente es el mecanismo de liberación de fármacos: aunque se ha demostrado la capacidad de cargar moléculas, habrá que optimizar las dosis y los tiempos de liberación para que resulten terapéuticamente eficaces. Finalmente, se investiga la posibilidad de usar espermatozoides vivos magnetizados, lo que abriría la puerta no solo a la manipulación externa, sino también a la fertilización asistida directa.
No cabe duda de que este trabajo marca un hito en la convergencia entre biología y robótica médica. Convertir espermatozoides en vehículos guiados por campos magnéticos y visibles bajo rayos X no es solo una demostración de ingeniería sofisticada; es un posible salto cualitativo en el modo en que entendemos y tratamos la fertilidad y la salud reproductiva.
Como señala Khalil, «estamos convirtiendo los propios sistemas de transporte celular de la naturaleza en microrobots programables». La frase sintetiza la ambición de un proyecto que busca aprovechar lo mejor de la biología y la tecnología médica para resolver algunos de los problemas más complejos.
Queda camino por recorrer, pero la idea de que en un futuro cercano los médicos puedan guiar enjambres de microrobots espermáticos hasta un tumor uterino para liberar fármacos o hasta una trompa de Falopio para facilitar la concepción, ya no pertenece únicamente a la ciencia ficción. Con cada avance, la frontera entre lo biológico y lo tecnológico se difumina un poco más, ofreciendo soluciones innovadoras a la infertilidad y a enfermedades ginecológicas de difícil tratamiento. ▪️
Información facilitada por el TechMed Centre
Fuente: Magdanz, V., van der Mijle Meijer, J. K., Ligtenberg, L.J. W. et al. Sperm cell empowerment: X-ray-guided magnetic fields for enhanced actuation and localization of cytocompatible biohybrid microrobots. npj Robot (2025). DOI: https://doi.org/10.1038/s44182-025-00044-1