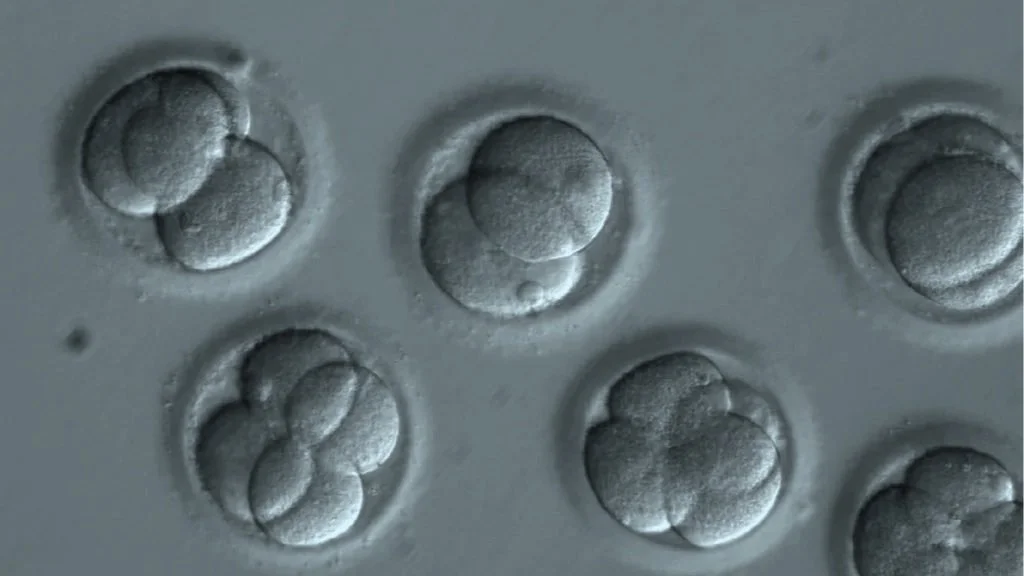
Los embriones masculinos se desarrollan más rápido que los femeninos, y ahora ya sabemos por qué
Un nuevo estudio revela que, desde los primeros días de vida, los embriones no siguen el mismo ritmo: los machos pisan el acelerador metabólico mientras las hembras priorizan el control y la regulación. La genética —y no las hormonas— tiene gran parte de la respuesta.
Por Enrique Coperías
Los embriones masculinos crecen más rápido que los femeninos desde el inicio: la clave está en sus genes, no en las hormonas, advierte un nuevo estudio. En la imagen, embrión quimérico de ratón, con células de rata. Cortesía: Salk Institute
En la biología del desarrollo hay un misterio que ha fascinado durante décadas a genetistas, veterinarios y especialistas en fertilidad: los embriones masculinos parecen ir con muchas prisa desde el principio.
Antes incluso de que se formen las gónadas y de que entren en juego las hormonas sexuales, los embriones macho y hembra muestran diferencias en la velocidad de desarrollo, como es la llegada a la fase de blastocisto. Esta es una etapa temprana del desarrollo embrionario, que ocurre unos 5 a 7 días después de la fecundación y en la que el embrión ya tiene entre cien y doscientas células.
Un estudio reciente liderado por investigadores de la Universidad Cornell, en Estados Unidos, y publicado en la revista Cell & Bioscience arroja nueva luz sobre este curioso fenómeno. Mediante un exhaustivo análisis del transcriptoma —es decir, del conjunto de genes activos— de embriones bovinos producidos in vitro, el equipo de científicos ha logrado describir con detalle qué engranajes moleculares marcan el compás más acelerado de los embriones varones.
«Entender estas diferencias fundamentales entre sexos a nivel genómico y molecular es de vital importancia para mejorar el éxito de la fecundación in vitro (FIV), tanto en seres humanos como en el ganado, así como para desarrollar tratamientos contra la infertilidad que funcionen en hombres y en mujeres», explica Jingyue Ellie Duan, profesora de Genómica Funcional en la Facultad de Agricultura y Ciencias de la Vida de Cornell y coautora del trabajo. Los primeros firmantes del trabajo son Meihong Shi, investigadora posdoctoral, y Guangsheng Li, doctorando, ambos en su laboratorio.
Una carrera desigual desde el inicio
Lo primero que confirma este trabajo es una observación que se repite en múltiples especies: en condiciones de cultivo in vitro, los embriones masculinos alcanzan la fase de blastocisto expandido con mayor frecuencia y rapidez que los femeninos. Hablamos de una fase del blastocisto en la que la cavidad interna —el blastocele— se llena de más líquido y se agranda, lo que hace que el embrión aumente de tamaño y la capa externa de células, el denominado trofoectodermo, se estire y adelgace. Es un paso previo a la implantación en el útero.
Duan y su equipo analizaron 444 embriones bovinos producidos a partir de óvulos procedentes del matadero y semen congelado de toros sementales. Tras sexarlos mediante pruebas de PCR (reacción en cadena de la polimerasa), comprobaron que en el día séptimo de desarrollo, más de dos tercios de los blastocistos expandidos eran machos. En el día octavo, la diferencia era aún más marcada, con proporciones de hasta cinco machos por cada hembra.
Esto sugiere que, incluso sin influencia hormonal, el motor genético masculino está más acelerado. La pregunta que cabe hacerse qué impulsa esta diferencia entre embriones.
La lupa en el transcriptoma
Para responder a este interrogante, Duan, Shi, Le y sus colegas recurrieron a dos tecnologías de secuenciación complementarias:
✅ La RNA-seq de lectura corta, que permite cuantificar con gran precisión qué genes se expresan y en qué nivel.
✅ La lectura larga (PacBio Iso-seq), que, dicho de forma sencilla, permite observar las moléculas de ARN de principio a fin, lo que facilita detectar versiones completas de los genes —llamadas isoformas— y variaciones en su empalme que suelen pasar desapercibidas con la técnica de lectura corta.”
De este modo, los investigadores no solo vieron qué genes se activaban de forma distinta entre machos y hembras, sino también cómo esos genes se cortan y empalman de maneras diferentes (splicing alternativo) y qué versiones completas de cada gen (isoformas) estaban presentes, procesos fundamentales para regular cómo progresa el desarrollo embrionario.
Metabolismo vs. vigilancia celular
En palabras de Duan, el hallazgo central de la investigación es que los embriones masculinos activan de manera preferente genes asociados al metabolismo energético. En ellos se encienden rutas de síntesis de aminoácidos, procesos mitocondriales y vías de obtención de energía. Entre los genes destacados figuran los que sintetizan enzimas como la SHMT2 y la ENO3. Estas están relacionadas con el metabolismo del carbono y la respiración celular.
En cambio, los embriones femeninos muestran mayor actividad en genes vinculados a procesos regulatorios y de control de calidad, como la vigilancia del ARN, la señalización TGF-beta /una vía de comunicación entre células que regula procesos clave como el crecimiento, la división, la diferenciación y la muerte celular— y rutas relacionadas con la diferenciación de las gónadas femeninas, esto es, los ovarios, y la respuesta inflamatoria.
Por tanto, podemos decir que los embriones masculinos apuestan por pisar el acelerador metabólico, mientras que los embriones femeninos invierten más recursos en sistemas de supervisión y regulación. Esta diferencia de estrategia podría explicar por qué los primeros avanzan más deprisa, aunque no necesariamente con mejor calidad embrionaria.
Cromosoma X, una ventaja que ralentiza a las hembras
Un aspecto crucial del estudio fue analizar cómo se compensa la dosis de genes ligados al cromosoma X. Las hembras poseen dos copias de este cromosoma, mientras que los machos solo una. En teoría, la inactivación del cromosoma X en las hembras debería equilibrar la balanza, pero en etapas tempranas este mecanismo aún no está completamente establecido.
Los autores encontraron que en los blastocistos femeninos la relación entre la expresión de genes del cromosoma X y de los autosomas —los cromosomas que no determinan el sexo—era mayor de lo esperado. Esta desproporción se debe a que numerosos genes escapan a la inactivación del cromosma X, de modo que las hembras tienen una dosis extra de genes. Entre ellos destacan candidatos como el MED12 y el SMARCA1, directamente implicados en la regulación del desarrollo embrionario.
«Estos datos podría implicar que existe un factor intrínseco en nuestro genoma que contribuye a las diferencias basadas en el sexo que observamos —como los cromosomas sexuales (XX frente a XY) o genes ligados al sexo— y no solo a cambios hormonales o a factores ambientales —apunta Duan. Y añade—: Nacemos con esta regulación genética específica de sexo que contribuye de manera muy distinta al comportamiento celular, al inicio de enfermedades y al desarrollo del sistema inmunitario, y que continúa a lo largo de toda la vida hasta afectar a la salud y al envejecimiento».
El nuevo descubrimiento podría tener interesantes aplicaciones en medicina reproductiva humana, ya que comprender mejor las diferencias entre sexos en las primeras etapas de la vida podría explicar por qué algunos embriones in vitro prosperan más que otros, y podría servir para afinar los criterios de selección en clínicas de fertilidad. Cortesía: Universidad de Ciencia y Salud de Oregón
El rompecabezas del splicing alternativo
Otra elemento a tener en cuenta en este desfase embrionario es lo que se conoce como empalme o splicing alternativo. Este es un mecanismo que permite a un mismo gen generar distintas versiones. Los investigadores detectaron más de 1.500 diferencias de este tipo entre embriones macho y hembra; la más común fue los llamados exones saltados, fragmentos de información genética que a veces se usan y otras se descartan.
Más de 1.500 eventos de splicing resultaron ser diferentes entre uno y otro sexo; de ellos, predominaban los exones saltados o saltos de exón. En los embriones masculinos, estos eventos se asociaban a genes del metabolismo y del procesamiento del ARN, mientras que en los femeninos estaban vinculados a la síntesis de péptidos y las funciones regulatorias.
Además, los investigadores identificaron proteínas reguladoras del splicing con sesgo sexual. Por ejemplo, la FMR1 y la HNRNPH2, conocidas por su papel en enfermedades humanas como el síndrome X frágil, aparecieron más activas en embriones femeninos. Esto sugiere que el control del splicing es un terreno donde los embriones hembra despliegan más sofisticación, aunque a costa de velocidad de desarrollo.
Un fenómeno conservado en mamíferos
Gracias a la secuenciación de lectura larga, Duan y sus colegas descubrieron más de 140.000 isoformas nuevas en los embriones bovinos tempranos. De ellas, por encima de un millar mostraron expresión diferencial entre sexos.
Los embriones masculinos tendían a favorecer isoformas asociadas a metabolismo y procesos de degradación de nutrientes, mientras que los femeninos se inclinaban por isoformas reguladoras que frenan la transcripción o la biosíntesis. Este hallazgo refuerza la idea de que los machos priorizan la energía inmediata para dividirse más rápido, mientras que las hembras mantienen un control de calidad celular más riguroso.
Aunque el trabajo estaba centrado en toros y vacas, los autores subrayan que la aceleración masculina es un fenómeno documentado en ratones, cerdos, ovejas e incluso en seres humanos. En nosotros la situación es más compleja: algunos estudios en embriones humanos procedentes de FIV no detectan sesgos claros, mientras que otros sí observan ventajas en los masculinos, dependiendo de las condiciones de cultivo.
Lo interesante es que las bases moleculares parecen conservarse: activación metabólica en machos frente a regulación y vigilancia en hembras.
Implicaciones prácticas
Más allá de la curiosidad científica, estos hallazgos tienen aplicaciones directas:
✅ Ganadería: conocer qué factores influyen en la velocidad de desarrollo embrionario puede ayudar a optimizar técnicas de reproducción asistida, mejorar tasas de implantación y ajustar el sexado de embriones.
✅ Medicina reproductiva humana: comprender las diferencias tempranas entre sexos puede explicar por qué algunos embriones in vitro prosperan más que otros, y podría servir para afinar los criterios de selección en clínicas de fertilidad.
✅ Biomedicina: el descubrimiento del splicing y de las isoformas con sesgo sexual en etapas precoces abre nuevas líneas de investigación sobre enfermedades ligadas al sexo y trastornos del desarrollo.
Duan destaca un aspecto de su trabajo que trasciende a la embriología: «La diferencia de sexo ha sido un factor ignorado en muchos estudios y ensayos clínicos. Hasta hace muy poco, la mayoría de las investigaciones en ratones se hacía exclusivamente con machos. Y la mayoría de la búsqueda de fármacos también se basa en ratones machos. Sin embargo, vemos que la aparición y la frecuencia de muchas enfermedades son distintas en hombres y mujeres: el alzhéimer, ciertas enfermedades autoinmunes, las cardiopatías. En este estudio básico encontramos que los embriones masculinos y femeninos son diferentes incluso en esta etapa tan temprana, en función de la regulación del genoma».
Velocidad no siempre significa calidad embrionaria
Un aspecto que los autores recalcande este hallazgo es que avanzar más rápido no necesariamente es sinónimo de mejor salud embrionaria. En ratones, por ejemplo, los embriones que se desarrollan demasiado deprisa presentan más errores de impronta genética y mayores tasas de anomalías cromosómicas.
En los seres humanos, las evidencias apuntan a que un desarrollo intermedio puede ser el más favorable para la implantación y el éxito de la gestación.
Así, los embriones masculinos quizá ganan la carrera en velocidad de desarrollo, pero las hembras podrían estar construyendo, a un ritmo más pausado, una base más sólida para la viabilidad a largo plazo. Podría decirse que los machos corren y las hembras calibran. Dos estrategias distintas para afrontar el mismo viaje hacia la vida. ▪️
Información facilitada por la Universidad Cornell
Fuente: Shi, M., Li, G., Araujo, H. M. et al. Sex-biased transcriptome in in vitro produced bovine early embryos. Cell & Bioscience (2025). DOI: https://doi.org/10.1186/s13578-025-01459-x