Cómo el trasplante fecal puede potenciar la inmunoterapia contra el cáncer
Un ensayo clínico demuestra que el trasplante de microbiota fecal puede duplicar el tiempo de control del cáncer de riñón metastásico en pacientes tratados con inmunoterapia. El estudio refuerza el papel clave del intestino y de la microbiota intestinal en la respuesta a los tratamientos oncológicos.
Por Enrique Coperías, periodista científico
Las bacterias presentes en las heces podrían ser un arma inesperada en la lucha contra el cáncer. Foto: National Cancer Institute
Uno de los hitos fundacionales de la inmunoterapia contra el cáncer se remonta a 1957, cuando los científicos Lewis Thomas y Frank M. Burnet formularon la teoría de la inmunovigilancia del cáncer. Su idea, tan sencilla como revolucionaria, proponía que el sistema inmunitario no es un espectador pasivo, sino un vigilante activo: los linfocitos —un tipo de glóbulo blanco— patrullan el organismo como perros guardianes, capaces de detectar y eliminar células que han sufrido mutaciones peligrosas antes de que se conviertan en un tumor.
Aquella intuición contenía una promesa de enorme alcance: si el sistema inmunitario ya sabía reconocer el cáncer, quizá la medicina pudiera aprender a reforzar, guiar o reactivar ese mecanismo natural de defensa. Durante años, la inmunoterapia ha sido presentada como una de las grandes revoluciones en la lucha contra el cáncer.
Fármacos capaces de despertar al sistema inmunitario para que ataque a las células tumorales han cambiado el pronóstico de enfermedades antes casi siempre mortales. Sin embargo, el entusiasmo inicial ha dado paso a una realidad más compleja: no todos los pacientes responden igual. En muchos casos, el tumor acaba encontrando la forma de esquivar el ataque inmunitario. Ahora, una línea de investigación tan inesperada como prometedora apunta al interior del intestino humano como posible aliado para mejorar esos tratamientos.
El intestino como aliado inesperado contra el cáncer
«Se sabe que la microbiota intestinal influye en el sistema inmunitario y, en el cáncer de riñón, varios factores, como la intensa angiogénesis —formación de nuevos vasos sanguíneos a partir de otros ya existentes— y los mediadores inflamatorios, como la interleucina 6, pueden reducir la eficacia de la inmunoterapia», explica Giampaolo Tortora, catedrático de Oncología Médica en la Università Cattolica del Sacro Cuore y director del Comprehensive Cancer Centre del Hospital Gemelli, en Italia.
Un ensayo clínico publicado en la revista Nature Medicine ha mostrado que los trasplantes de microbiota fecal —una técnica que consiste en transferir bacterias intestinales de una persona sana o especialmente seleccionada a otra— podrían aumentar de forma significativa la eficacia de la inmunoterapia en pacientes con cáncer renal metastásico.
El estudio sugiere que modificar el ecosistema microbiano del intestino puede marcar la diferencia entre que un tratamiento funcione durante unos meses o logre mantener la enfermedad controlada durante años.
La microbiota intestinal contra los tumores malignos
El trabajo se centra en el carcinoma de células renales metastásico, la forma más frecuente de cáncer de riñón avanzado. En la última década, el tratamiento estándar de primera línea para muchos de estos pacientes combina dos fármacos:
✅ El pembrolizumab, un inhibidor de puntos de control inmunitario.
✅ El axitinib, un medicamento que bloquea la formación de nuevos vasos sanguíneos en el tumor.
Esta combinación ha mejorado la supervivencia, pero la mayoría de los pacientes acaba sufriendo una progresión de la enfermedad en poco más de un año.
La pregunta que se plantearon los investigadores fue sencilla y audaz a la vez: ¿y si parte de la culpa de esa falta de respuesta estuviera en el intestino? Cada persona alberga en su aparato digestivo billones de bacterias, virus y hongos que forman la llamada microbiota. En los últimos años, numerosos estudios han demostrado que este ecosistema influye de manera decisiva en el sistema inmunitario. También se había observado que los pacientes tratados con antibióticos —que alteran profundamente la microbiota— respondían peor a la inmunoterapia. La hipótesis parecía clara: ciertas comunidades bacterianas podrían facilitar, o dificultar, la acción de estos fármacos.
🗣️ «Nuestra hipótesis de trabajo era que trasplantar una microbiota intestinal favorable podía potenciar la respuesta a la inmunoterapia», señala Gianluca Ianiro, investigador principal del estudio, investigador en Enfermedades Digestivas en la Università Cattolica del Sacro Cuore y médico del CEMAD del Hospital Gemelli.
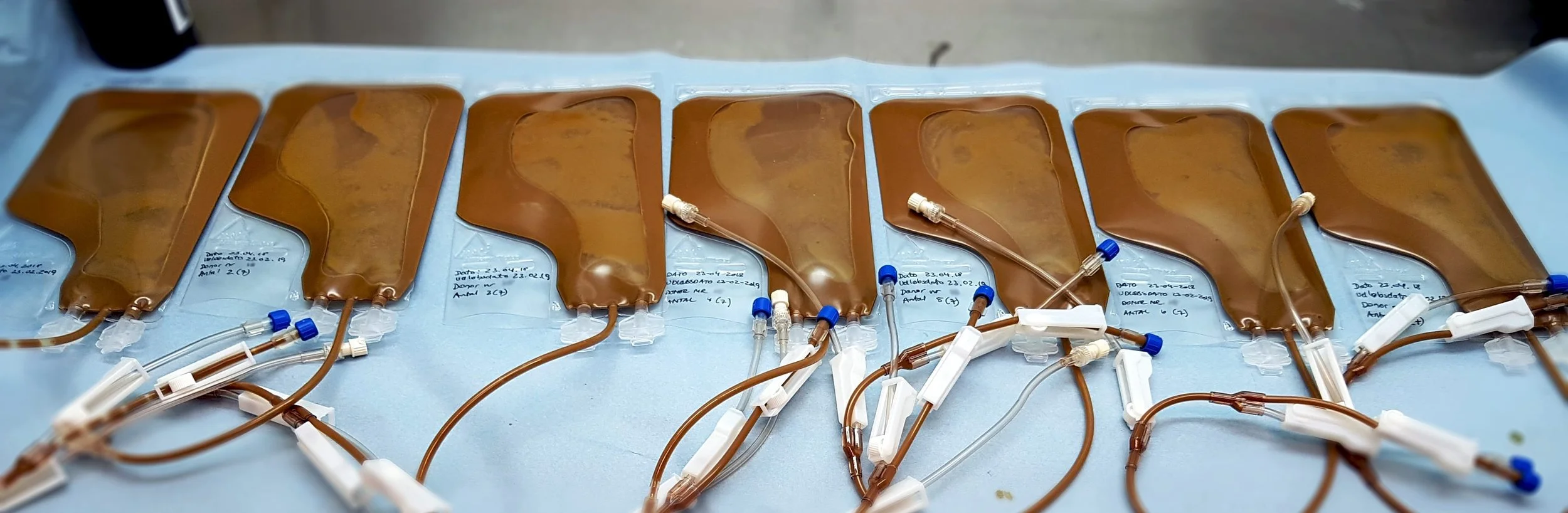
Un ensayo clínico muestra que el trasplante de microbiota fecal puede reforzar la eficacia de la inmunoterapia contra el cáncer. La técnica, aún experimental, ha logrado prolongar el control de la enfermedad en pacientes con cáncer renal avanzado. Cortesía: Simon Mark Dahl Jørgensen / GP Medical Devices
El ensayo TACITO: cómo se diseñó el estudio
Para comprobarlo, el equipo diseñó el ensayo clínico TACITO, un estudio aleatorizado, doble ciego y controlado con placebo. En él participaron 45 pacientes con cáncer renal metastásico que no habían recibido tratamientos previos. Todos fueron tratados con pembrolizumab y axitinib, pero además recibieron tres intervenciones adicionales a lo largo de seis meses.
La mitad de ellos recibió un trasplante de microbiota fecal procedente de donantes muy específicos: pacientes con el mismo tipo de cáncer que habían logrado una respuesta completa y duradera a la inmunoterapia. El resto recibió un trasplante placebo, indistinguible en la forma, pero sin microbiota activa.
🗣️ «TACITO es el primer ensayo aleatorizado en el mundo que compara los resultados de la inmunoterapia tras un trasplante de microbiota fecal procedente de pacientes respondedores frente a un placebo», subraya el propio Ianiro.
Resultados: más tiempo sin progresión del cáncer
Los resultados de la investigación fueron llamativos. Aunque el objetivo principal del estudio —el porcentaje de pacientes sin progresión de la enfermedad al cabo de doce meses— no alcanzó el umbral estadístico clásico por muy poco, las diferencias entre ambos grupos fueron clínicamente relevantes.
Siete de cada diez pacientes que recibieron el trasplante real seguían sin progresión al año, frente a poco más de cuatro de cada diez en el grupo placebo. Más aún, cuando se analizó el tiempo medio hasta que la enfermedad volvió a avanzar, la diferencia fue contundente: dos años en el grupo con trasplante de microbiota frente a solo nueve meses en el grupo control.
🗣️ «En particular, la mediana de la supervivencia libre de progresión fue claramente más larga en el grupo que recibió el trasplante de microbiota: veinticuatro meses frente a nueve meses en el grupo control, lo que equivale a una reducción del 50% en el riesgo de progresión de la enfermedad», destaca Roberto Iacovelli, coinvestigador principal y profesor asociado de Oncología en la Università Cattolica del Sacro Cuore.
En otras palabras, añadir el trasplante fecal al tratamiento estándar duplicó, de media, el tiempo durante el cual el cáncer permaneció controlado. También se observó una mayor tasa de respuesta tumoral: el 52% de los pacientes del grupo experimental experimentó una reducción significativa del tumor, frente al 32% en el grupo placebo. La supervivencia global fue también mayor en el grupo tratado con microbiota, aunque el estudio no tenía suficiente tamaño como para demostrar una diferencia estadísticamente sólida en este punto.
Qué bacterias importan y por qué
Más allá de los números, el trabajo aporta pistas sobre el cómo y el por qué de estos efectos. Los investigadores analizaron cientos de muestras de heces a lo largo del estudio para observar cómo cambiaba la microbiota intestinal de los pacientes. Confirmaron que las bacterias de los donantes lograban implantarse en el intestino de los receptores y que esa colonización iba acompañada de un aumento de la diversidad microbiana, un rasgo que suele asociarse con mejor salud intestinal.
Sin embargo, uno de los hallazgos más interesantes fue que no bastaba con que las bacterias del donante se instalaran en el nuevo huésped. Lo crucial parecía ser qué bacterias concretas aparecían… y cuáles desaparecían.
El equipo de investigación identificó ciertas especies cuya presencia temprana tras el trasplante de microbiota fecal se asociaba con mejores resultados clínicos, y otras cuya colonización se vinculaba con una peor evolución. Esto refuerza la idea de que no existe una microbiota buena universal, sino combinaciones complejas que interactúan con el sistema inmunitario y el tumor de formas todavía poco comprendidas.
Seguridad del trasplante de microbiota fecal
Los beneficios del trasplante fecal fueron especialmente claros en los pacientes con pronóstico intermedio o desfavorable, un grupo que suele tener menos opciones terapéuticas y peores resultados clínicos.
«Este hallazgo es especialmente relevante, ya que estos pacientes suelen disponer de menos opciones terapéuticas y presentan peores resultados clínicos», apunta Chiara Ciccarese, coautora principal del estudio e investigadora en oncología en la Università Cattolica del Sacro Cuore.
En términos de seguridad, el procedimiento resultó tranquilizador. Los trasplantes fecales fueron bien tolerados y no se detectaron infecciones ni efectos adversos graves atribuibles directamente a la microbiota transferida. Los efectos secundarios observados fueron los esperables del tratamiento oncológico estándar y no se incrementaron de forma significativa en el grupo que recibió el trasplante real.
🗣️ «Las muestras de los donantes se sometieron a un exhaustivo cribado clínico y microbiológico, que incluyó pruebas frente a agentes patógenos bacterianos, víricos y parasitarios —explica Maurizio Sanguinetti, catedrático de Microbiología en la Università Cattolica del Sacro Cuore. Y añade—: Todos los procedimientos se llevaron a cabo en entornos controlados para minimizar los riesgos infecciosos».
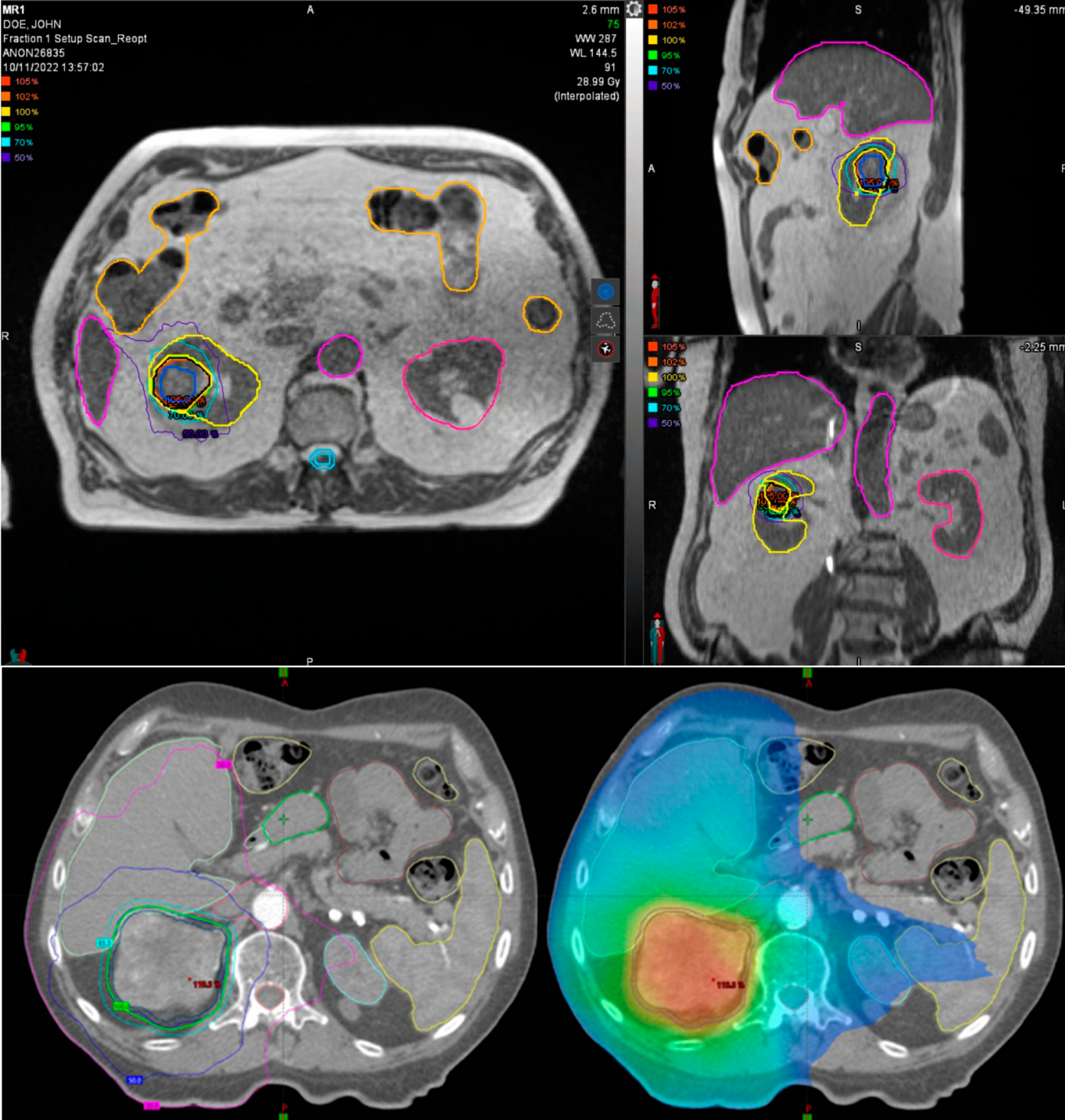
Esquema del tratamiento de radioterapia ablativa estereotáxica (SABR) en pacientes con cáncer renal. Esta técnica de alta precisión se utiliza en el carcinoma de células renales para destruir el tumor con dosis concentradas de radiación, y forma parte del arsenal terapéutico que, junto a la inmunoterapia y nuevas estrategias como la modulación de la microbiota intestinal, busca mejorar el control de la enfermedad. Cortesía: Cancers / https://doi.org/10.3390/cancers16152678
Una pieza clave en la respuesta inmunoilógica
Los autores del estudio son prudentes en sus conclusiones. Reconocen que el número de pacientes es reducido y que la mayoría de las muestras fecales procedían de un único donante, lo que limita la generalización de los resultados.
También señalan que el estudio se inició antes de que se popularizara el uso de antibióticos para preparar el intestino antes de un trasplante fecal, una estrategia que podría aumentar aún más la eficacia de la intervención.
Aun así, el mensaje de fondo es potente: la microbiota intestinal no es un actor secundario, sino una pieza clave en la respuesta a la inmunoterapia. Modificarla de forma dirigida podría convertirse en una nueva herramienta para personalizar los tratamientos contra el cáncer. En lugar de centrarse solo en el tumor o en el sistema inmunitario, la oncología del futuro podría tener que mirar también —y muy en serio— al intestino.
Qué significa este hallazgo para el futuro del cáncer
«Estos resultados aportan más pruebas de que la microbiota intestinal es un modulador clave de la respuesta a la inmunoterapia —explica Ianiro. Y concluye—: El trasplante de microbiota fecal procedente de donantes cuidadosamente seleccionados podría convertirse en una estrategia complementaria importante para mejorar los resultados en el carcinoma renal metastásico, probablemente al proporcionar un estímulo inmunológico que refuerza la respuesta al tratamiento».
El siguiente paso será confirmar estos resultados en ensayos más amplios y explorar alternativas más estandarizadas, como consorcios bacterianos o medicamentos vivos que eviten las dificultades logísticas y éticas del trasplante fecal tradicional. Si estos estudios confirman lo observado, la idea de que unas bacterias bien elegidas puedan ayudar al cuerpo a combatir el cáncer dejará de sonar extravagante para convertirse en una nueva frontera de la medicina.
Por ahora, el ensayo TACITO aporta una prueba convincente de que, en la batalla contra el cáncer, a veces el aliado más inesperado puede encontrarse en el lugar más insospechado. En el complejo diálogo entre el tumor, el sistema inmunitario y los microorganismos que nos habitan, el intestino empieza a reclamar un papel protagonista.▪️(30-enero-2026)
TAMBIÉN TE PUEDE INTERESAR:
🩻 El laxante que podría retrasar la diálisis en pacientes con enfermedad renal crónica
Información facilitada por la Universita Cattolica del Sacro Cuore
Fuente: Porcari, S., Ciccarese, C., Heidrich, V. et al. Fecal microbiota transplantation plus pembrolizumab and axitinib in metastatic renal cell carcinoma: the randomized phase 2 TACITO trial. Nature Medicine (2026). DOI: https://doi.org/10.1038/s41591-025-04189-2