Cómo los genes moldean nuestro microbioma intestinal: científicos descubren once variantes genéticas con impacto en la salud
Durante años se pensó que la microbiota intestinal dependía sobre todo de la dieta y el entorno. Ahora, dos grandes estudios confirman que nuestros genes también deciden qué bacterias viven en el intestino y cómo influyen en la salud.
Por Enrique Coperías, periodista científico
Un equipo de científicos ha hallado once variantes genéticas que influyen en la microbiota intestinal humana y en el riesgo de padecer determinadas enfermedades. Se trata del mayor estudio sobre genética y microbioma. Crédito: IA-DALL-E-RexMolón Producciones
El mayor estudio hasta ahora sobre genes y microbioma intestinal
La microbiota intestinal se nos ha presentado de forma tradicional como un ecosistema moldeado sobre todo por la dieta, el estilo de vida y el entorno. Sin embargo, una nueva generación de estudios empieza a descubrir que también hay un director de orquesta menos visible: nuestros propios genes.
Dos investigaciones publicadas en la revista Nature Genetics acaban de aportar la evidencia más sólida hasta la fecha de que el ADN humano influye de forma directa y medible en la composición de las bacterias intestinales que habitan el intestino.
En conjunto, los trabajos identifican once variantes genéticas que afectan al microbioma intestinal humano y dibujan un mapa más preciso de cómo el organismo y sus microorganismos coevolucionan. El hallazgo no solo añade complejidad a la relación entre genética y salud, sino que abre la puerta a una medicina de precisión en la que microbioma y genoma se estudien como un sistema integrado.
¿Qué es la microbiota intestinal y por qué es importante?
La microbiota intestinal es una comunidad extraordinariamente diversa de bacterias, virus, hongos y otros microorganismos que habitan de forma estable en el tracto digestivo humano y que, lejos de ser simples pasajeros, desempeñan funciones esenciales para el organismo. Participan en la digestión de alimentos que el cuerpo no puede descomponer por sí solo, contribuyen a la síntesis de vitaminas y metabolitos fundamentales, modulan el metabolismo energético y ayudan a mantener el equilibrio del sistema inmunitario.
También intervienen en la integridad de la barrera intestinal, la comunicación entre intestino y cerebro —el llamado eje intestino-cerebro— y en la producción de compuestos químicos que influyen en procesos inflamatorios y hormonales.
Este ecosistema microbiano, que contiene billones de microorganismos y miles de especies diferentes, es tan complejo que a menudo se describe como un órgano invisible más del cuerpo humano. Su composición varía de una persona a otra y cambia a lo largo de la vida en función de factores como la dieta, el entorno, la edad, el uso de medicamentos —especialmente antibióticos—, el estilo de vida o la exposición a agentes patógenos.
Primeros pinitos: los genes de la lactasa y el sistema sanguíneo ABO
En la última década, la irrupción de las técnicas de secuenciación genética masiva ha permitido estudiar el microbioma con una precisión sin precedentes, revelando de este modo su relación con enfermedades metabólicas como la obesidad y la diabetes, trastornos autoinmunes, afecciones gastrointestinales e incluso alteraciones neurológicas y psiquiátricas.
Este creciente interés científico ha consolidado la idea de que la microbiota intestinal no solo refleja el estado de salud, sino que también puede influir activamente en él. Sin embargo, a pesar de los avances en la comprensión de cómo la dieta o el entorno modifican el microbioma, hasta hace poco se sabía relativamente poco sobre el papel que desempeña la genética humana en su configuración.
Una de las dificultades ha sido técnica. Los primeros estudios que intentaron relacionar genes humanos y microbioma utilizaron métodos de secuenciación limitados, con baja resolución para identificar bacterias a nivel de especie. Además, cada investigación empleaba protocolos distintos, lo que dificultaba comparar resultados.
Por eso, durante años solo se habían identificado con solidez dos regiones genéticas asociadas de forma reproducible con el microbioma intestinal: el gen de la lactasa, relacionado con la digestión de la leche; y el sistema sanguíneo ABO, la clasificación de los grupos sanguíneos humanos en A, B, AB y O según las moléculas (antígenos) presentes en la superficie de los glóbulos rojos.
El cuerpo humano no solo alberga bacterias: también posee sensores genéticos capaces de detectar sus señales químicas y modular el entorno intestinal, favoreciendo a unas especies microbianas frente a otras. Crédito: IA-Grok-RexMolón-Producciones
El mayor estudio hasta ahora sobre genes y microbioma intestinal
Los dos nuevos trabajos amplían de forma significativa ese panorama. El primero, liderado por equipos suecos y basado en datos de más de 16.000 personas, analizó el microbioma intestinal mediante secuenciación metagenómica de alta resolución y buscó asociaciones con millones de variantes genéticas humanas.
Los resultados se replicaron en una cohorte independiente de más de 12.000 participantes noruegos.
El segundo estudio, centrado en el gran proyecto sanitario noruego Trøndelag Health Study o HUNT, examinó también miles de genomas y microbiomas con técnicas similares y confirmó buena parte de los hallazgos.
Once variantes genéticas que influyen en las bacterias del intestino
Entre ambos trabajos, los científicos han conseguido identificar once variantes genéticas con efectos reproducibles sobre especies bacterianas concretas o sobre la diversidad global del microbioma. Algunas de ellas se sitúan en regiones ya conocidas, como los genes relacionados con la digestión de la lactosa o los grupos sanguíneos, pero otras son completamente nuevas.
Uno de los hallazgos más llamativos apunta a un locus genético —la posición concreta que ocupa un gen o una variante genética en un cromosoma— relacionado con receptores capaces de detectar ácidos grasos producidos por las bacterias intestinales. Estas moléculas, generadas durante la fermentación de la fibra dietética, actúan como señales químicas que influyen en la saciedad, la motilidad intestinal o la inflamación.
Pues bien, ciertas variantes en esta región del genoma aparecen vinculadas con cambios en la riqueza de especies del microbioma intestinal: cada copia de una de las versiones estudiadas se relaciona con una reducción medible en el número de especies bacterianas presentes.
Cómo los genes moldean el ecosistema del microbioma
Este resultado sugiere que el cuerpo humano no solo alberga microorganismos, sino que posee sensores específicos para escuchar sus señales químicas. Esos sensores, expresados en células del intestino que producen hormonas digestivas, podrían modular el entorno intestinal y favorecer a unas bacterias frente a otras. En otras palabras, la genética del huésped contribuiría a seleccionar qué microorganismos prosperan.
🗣️«Hemos aprendido mucho sobre el papel que desempeña la genética en el microbioma intestinal —dice Tove Fall, profesora de Epidemiología Molecular en la Universidad de Uppsala y responsable de uno de los estudios—. Y añade—: Varias de las conexiones genéticas que encontramos están relacionadas con mecanismos biológicos muy específicos. Tienen que ver, por ejemplo, con qué moléculas están presentes en la superficie de las células intestinales y, por tanto, disponibles como alimento para las bacterias. También se relacionan con la forma en que el intestino reacciona a las moléculas producidas por las bacterias».
Otro conjunto de variantes identificadas se relaciona con genes que determinan la composición del moco intestinal y de la superficie del epitelio digestivo. Este recubrimiento es el hábitat inmediato de muchas bacterias, que lo utilizan como fuente de nutrientes y como punto de anclaje. Cambios genéticos en proteínas del moco, como la mucina MUC12, se asocian con variaciones en la abundancia de especies concretas. En algunos casos, esas mismas variantes también se vinculan con enfermedades como las hemorroides, lo que sugiere un posible puente entre genética, microbioma y patología.
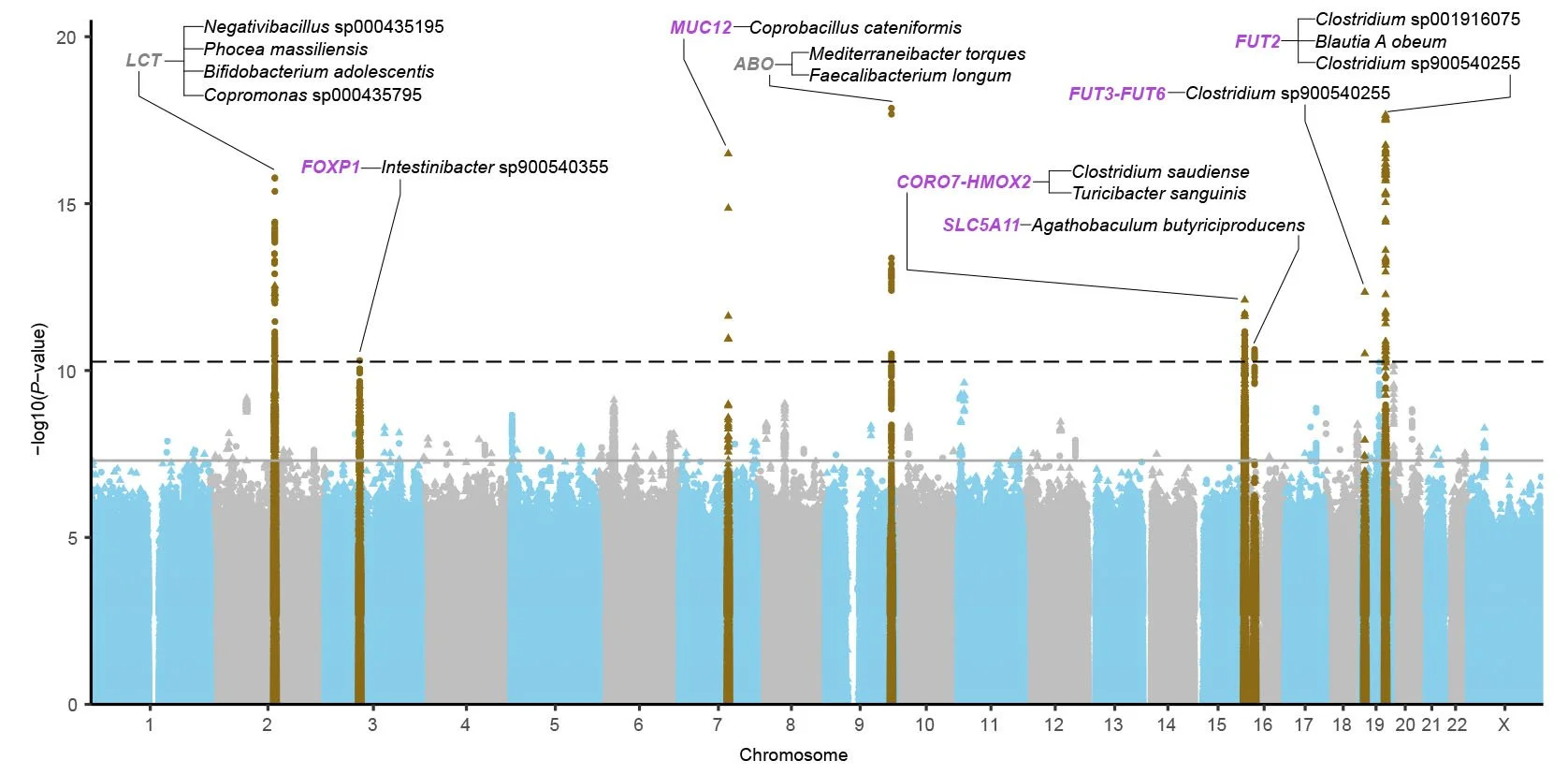
El gráfico muestra las asociaciones entre variantes genéticas humanas y 921 especies bacterianas del intestino en más de 16.000 participantes suecos: cada punto representa una variante genética y su relación con la microbiota, y las regiones genéticas identificadas por primera vez aparecen en color púrpura. Cortesía: Tove Fall, Universidad de Uppsala
Grupos sanguíneos y moco intestinal
El par de estudios también refuerza la importancia de los genes que regulan los antígenos de los grupos sanguíneos. Las moléculas que determinan si una persona es del grupo A, B, AB u O no solo están presentes en la sangre, sino también en el moco intestinal. Para muchas bacterias, estos antígenos son tanto alimento como superficie de adhesión.
Las variantes genéticas que controlan su producción influyen en la presencia de determinadas especies bacterianas, en un efecto que depende además de si la persona es secretora, es decir, si libera esos antígenos en sus fluidos corporales.
Este mecanismo ilustra de forma clara la interacción entre genética y microbioma. Al modificar los azúcares disponibles en el intestino, el ADN humano crea nichos ecológicos distintos que favorecen a unos microorganismos y dificultan a otros. Se estima que alrededor del 20% de las personas de ascendencia europea son no secretoras, lo que se traduce en perfiles microbianos diferentes.
Microbioma y capacidad de digerir la lactosa
El clásico gen de la lactasa vuelve a aparecer como uno de los actores principales. Las variantes que permiten digerir la lactosa en la edad adulta se asocian con cambios en varias especies bacterianas, incluidas algunas del género Bifidobacterium.
Este resultado se interpreta como una interacción entre dieta y genética: quienes pueden digerir lactosa consumen más productos lácteos, lo que altera el sustrato disponible para las bacterias intestinales.
Más allá de estas asociaciones concretas, los estudios estiman que la heredabilidad del microbioma —la proporción de su variación explicada por la genética— es moderada pero significativa. Dependiendo de la especie bacteriana, puede oscilar entre valores cercanos a cero y alrededor del 25%. Para la diversidad global de bacterias intestinales, la influencia genética se sitúa en torno al 15% o 20%. El resto depende de factores ambientales como la dieta, los medicamentos, el estilo de vida o la edad.
El índice de masa corporal puede influir de forma directa en la composición del microbioma intestinal, en una relación bidireccional en la que microbiota y obesidad se modifican mutuamente. Foto de Artem Podrez
Relación entre microbiota intestinal y riesgo de enfermedad
La interacción entre el microbioma y la salud aparece también en los análisis complementarios. Algunas variantes genéticas asociadas a bacterias concretas se vinculan a su vez con enfermedades autoinmunes o metabólicas. En el estudio noruego, por ejemplo, una variante relacionada con la abundancia de una bacteria intestinal se asocia con menor riesgo de diabetes de tipo 1 o enfermedad celíaca.
Aunque estos vínculos no implican causalidad directa, sugieren que el microbioma intestinal podría actuar como intermediario entre los genes y ciertas enfermedades.
En este sentido, los investigadores también detectaron conexiones claras entre algunas variantes genéticas y diversas patologías previamente relacionadas con el microbioma.
🗣️Como explica Claes Ohlsson, profesor de la Universidad de Gotemburgo y uno de los responsables del segundo estudio, «observamos que algunas de estas variantes genéticas estaban vinculadas al riesgo de intolerancia al gluten, hemorroides y enfermedades cardiovasculares. Esto sugiere que los cambios en la composición de las bacterias intestinales podrían ofrecer una vía para comprender mejor cómo los riesgos genéticos influyen en la salud».
Hacia una medicina personalizada basada en microbioma y genética
Otra línea de análisis indica que el índice de masa corporal puede influir de forma causal en la composición del microbioma, y no solo al revés. Esta relación bidireccional complica la clásica pregunta de si la microbiota determina la obesidad o si es esta la que modifica la microbiota. Probablemente ambas direcciones coexistan.
Los autores subrayan que aún queda mucho por entender sobre los mecanismos exactos. Identificar una asociación genética no implica conocer cómo se traduce en cambios biológicos concretos.
Sin embargo, la consistencia de los resultados en cohortes independientes y con técnicas de alta resolución sugiere que la influencia genética es real y relevante.
La implicación más prometedora es la posibilidad de integrar genómica y microbioma en la medicina personalizada. Si determinados perfiles genéticos predisponen a albergar comunidades bacterianas específicas, en el futuro podría diseñarse nutrición o tratamientos probióticos adaptados a cada individuo. También podría ayudar a predecir quién responderá mejor a terapias basadas en la microbiota.
«Dado que muchos aspectos de nuestra salud están relacionados con el microbioma intestinal, queremos naturalmente que nuestra investigación contribuya a mejorar las formas de prevenir y tratar enfermedades teniendo en cuenta la interacción entre los genes, la biología intestinal y el microbioma», concluye Fall.
Durante años, el microbioma se ha presentado como un órgano casi independiente, moldeado por lo que comemos y por el entorno. Los nuevos datos obligan a matizar esa visión. El intestino humano es un ecosistema compartido, donde genes y bacterias se influyen mutuamente. Y en ese diálogo continuo entre ADN humano y ADN microbiano podría esconderse una parte importante de la biología de la salud.▪️(13-febrero-2026)
Información facilitada por la Universidad de Uppsala
Fuente:
- Dekkers, K. F., Pertiwi, K., Baldanzi, G. et al. Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation. Nature Genetics (2026). DOI: https://doi.org/10.1038/s41588-026-02512-2
-Moksnes, M .R., Coward, E., Nethander, M. et al. The HUNT study identifies host genetic factors reproducibly associated with human gut microbiota composition. Nature Genetics (2026). DOI: https://doi.org/10.1038/s41588-026-02502-4