Nanotúneles celulares y enfermedad de Huntington: cómo un nuevo descubrimiento podría frenar su propagación
Los diminutos túneles invisibles que conectan unas neuronas con otras podrían estar propagando el daño en la enfermedad de Huntington. Ahora, un hallazgo científico identifica cómo bloquear ese mecanismo y abre una prometedora vía para frenar la progresión de este trastorno genético en el que las células nerviosas de ciertas partes del cerebro se desgastan o se degeneran.
Por Enrique Coperías, periodista científico
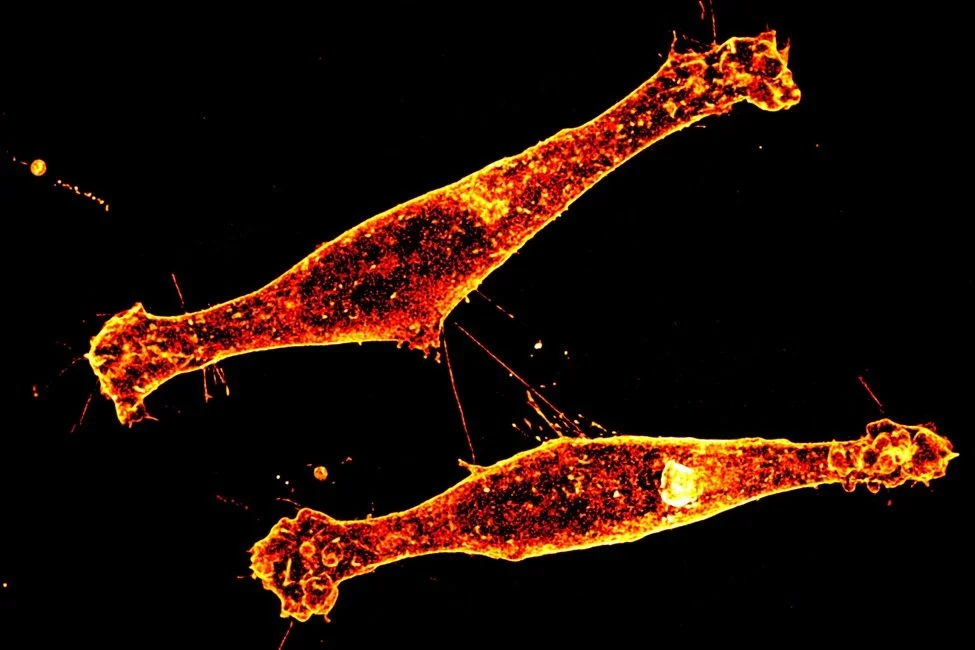
Nanotúneles celulares que conectan neuronas con expresión de Rhes, una proteína implicada en la propagación de la enfermedad de Huntington. Cortesía: FAU
La enfermedad de Huntington, también conocida como corea de Huntington, se ha entendido como un proceso íntimo, casi solitario: una mutación genética transmitida por el padre o la madre desencadena la producción de una proteína tóxica que, poco a poco, va destruyendo las neuronas.
Pero un nuevo estudio sugiere que este deterioro podría no ser tan aislado como se pensaba. En realidad, las células enfermas podrían estar contagiando a sus vecinas.
La investigación, publicada en la revista Science Advances, describe un hallazgo sorprendente: la existencia de diminutos puentes entre células —los llamados nanotubos de membrana— que permiten el paso de proteínas dañinas de una neurona a otra. Y, lo más relevante, identifica un mecanismo molecular clave que podría bloquear ese proceso.
¿Qué es la enfermedad de Huntington?
La enfermedad de Huntington es un trastorno neurodegenerativo hereditario poco frecuente que afecta aproximadamente a entre cinco y diez personas por cada 100.000 habitantes en Europa.
Está causada por una mutación en el gen HTT, que dirige la producción de una proteína anómala, la llamada huntingtina mutada, que se acumula y resulta tóxica para las neuronas, especialmente en regiones del cerebro implicadas en el movimiento, la conducta y la cognición.
Este trastorno se transmite de forma autosómica dominante, lo que significa que basta heredar una copia del gen alterado para desarrollar la enfermedad. Sus síntomas suelen aparecer en la edad adulta, generalmente entre los treinta y cuarenta años, e incluyen movimientos involuntarios (corea), alteraciones psiquiátricas, como depresión e irritabilidad, y un deterioro progresivo de las funciones cognitivas, como es la capacidad de pensar.
Existen medicamentos que ayudan a aliviar y controlar algunos síntomas de la enfermedad de Huntington, especialmente los movimientos involuntarios y las alteraciones psiquiátricas. Sin embargo, estos tratamientos son únicamente paliativos y no actúan sobre la causa del trastorno, por lo que no pueden detener ni revertir el deterioro progresivo —físico, cognitivo y conductual— que caracteriza a la enfermedad.
Huntington, una enfermedad que podría propagarse entre neuronas
En este contexto, comprender cómo se propaga el daño neuronal se ha convertido en una prioridad científica. Los nanotubos de membrana o citonemas son estructuras extremadamente finas —hasta 200 nanómetros de diámetro— que conectan directamente el interior de dos células vecinas. A través de ellos pueden viajar moléculas, vesículas e incluso orgánulos celulares.
No son una rareza: cada vez hay más evidencias de que desempeñan un papel importante en enfermedades neurodegenerativas.
El equipo liderado por Sunayana Dagar, del Departamento de Química/Bioquímica, en la Universidad Atlántica de Florida o FAU (Estados Unidos), ha demostrado que estos túneles funcionan como auténticas autopistas para la citada proteína mutadahuntingtina (mHTT), responsable de la enfermedad de Huntington. Esta proteína, una vez formada, no se queda confinada en la célula que la produce, sino que puede desplazarse a otras neuronas, extendiendo el daño.
«La propagación celular de la huntingtina mutada es un componente clave de la progresión de la enfermedad», señalan los autores . El hallazgo refuerza la idea de que algunas enfermedades neurodegenerativas comparten mecanismos similares a los de las infecciones, aunque sin virus ni bacterias de por medio.
El papel de Rhes, la proteína que construye los nanotúneles
El estudio se centra en una proteína conocida como Rhes, abundante en el cuerpo estriado, la región cerebral más afectada en el Huntington. Investigaciones previas ya habían sugerido que Rhes favorece la formación de estos nanotúneles y facilita el transporte de la proteína tóxica entre neuronas.
Ahora, los científicos han confirmado que Rhes no solo participa en el proceso, sino que actúa como un auténtico arquitecto de estas conexiones. En distintos modelos celulare, queincluyen neuronas humanas derivadas de células madre, observaron que la presencia de Rhes multiplicaba por cuatro la formación de nanotubos de membrana.
Además, estos túneles no son simples contactos superficiales. Experimentos con proteínas fluorescentes demostraron que permiten un intercambio directo de material entre células, lo que implica una continuidad funcional entre sus citoplasmas.
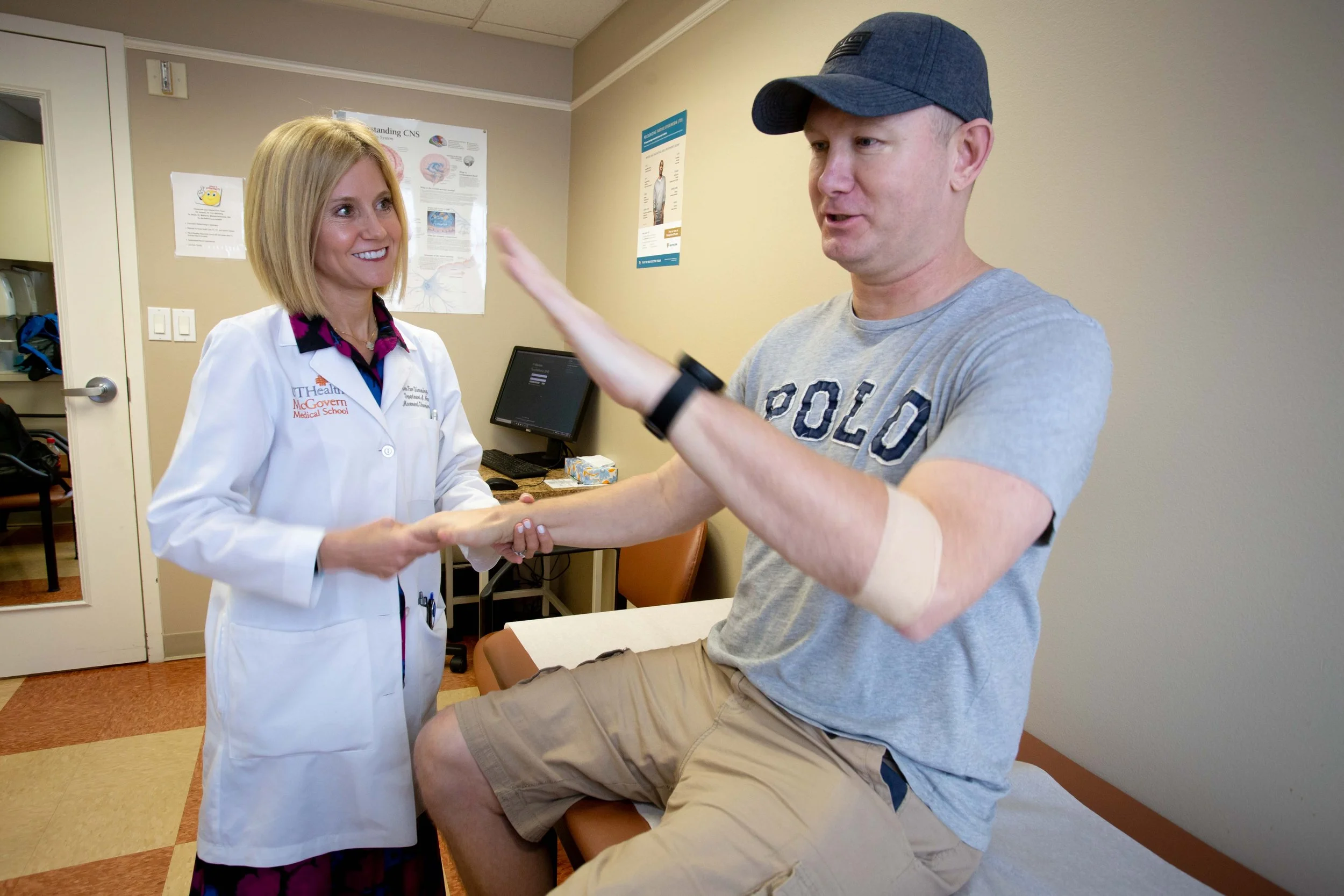
La neuróloga Erin Furr Stimming examina a un paciente con enfermedad de Huntington en UTHealth Houston, una dolencia neurodegenerativa cuya progresión podría estar relacionada con la propagación de proteínas tóxicas entre neuronas a través de nanotúneles celulares. Cortesía: Maricruz Kwon / UTHealth Houston
El sensor de pH Slc4a7, el nuevo objetivo terapéutico identificado
El avance más relevante del trabajo llega al identificar a un segundo actor clave: la proteína Slc4a7. Este transportador, conocido por regular el pH intracelular, aparece como un socio esencial de Rhes en la formación de los nanotúneles.
Mediante técnicas de proteómica, los investigadores detectaron que Slc4a7 es uno de los principales interactores de Rhes en la membrana celular. Cuando bloquearon su función —ya fuera mediante silenciamiento genético o fármacos— la formación de nanotúneles se redujo drásticamente .
El efecto fue contundente: menos túneles implicaban menos transferencia de la proteína tóxica entre células.
«Slc4a7 emerge como un regulador crítico de la formación de nanotúneles y del transporte intercelular de huntingtina mutada», podemos leer en el artículo científico.
🗣️ «Este trabajo cambia radicalmente nuestra forma de entender la progresión de la enfermedad de Huntington —afirma el doctor Srinivasa Subramaniam, autor principal, profesor del Departamento de Química y Bioquímica de la Facultad de Ciencias de la FAU. Y añade—: Sabíamos que las neuronas se transmiten proteínas tóxicas entre sí de alguna manera, pero ahora podemos ver el mecanismo que lo hace posible. Al identificar a SLC4A7 como un socio clave de Rhes, hemos descubierto una nueva diana, potencialmente susceptible de tratamiento farmacológico, para detener esa propagación en su origen».
Cómo se forman los nanotúneles: mecanismo explicado
El mecanismo descubierto tiene un componente físico y químico. Por un lado, Rhes se une directamente a Slc4a7 en la membrana celular. Por otro, esta interacción modifica el pH local, lo que crea un entorno más alcalino.
Ese cambio aparentemente sutil tiene consecuencias profundas: favorece la reorganización del citoesqueleto de actina, la estructura interna que permite a la célula generar prolongaciones y, en este caso, construir los nanotubos de membrana.
Es decir, el proceso no depende solo de la presencia de proteínas, sino de un microambiente químico que facilita la arquitectura celular.
Curiosamente, el estudio muestra que no es necesario que Slc4a7 transporte iones para unirse a Rhes, pero sí lo es para que se formen dichos nanotúneles. Esto sugiere que la interacción física y la función bioquímica son dos niveles distintos del mismo proceso.
Bloquear la propagación del Huntington: resultados en animales
El hallazgo más prometedor llega al trasladar estos resultados al cerebro vivo. En modelos de ratón modificados genéticamente para carecer de Slc4a7, la propagación de la proteína mutada desde el punto de inyección fue significativamente menor.
Mientras que en animales normales la huntingtina mutada se extendía hasta un milímetro de distancia, en los ratones sin Slc4a7 ese desplazamiento se redujo notablemente .
Este resultado es clave: demuestra que el mecanismo no es un artefacto de laboratorio, sino que también opera en el cerebro.
Además, el bloqueo de Slc4a7 no redujo la cantidad de proteína producida, sino su capacidad de propagarse. Esto abre una vía terapéutica distinta: no eliminar la causa genética —algo extremadamente complejo—, sino frenar la expansión del daño.
Nueva estrategia terapéutica: frenar la propagación, no solo la causa
Tradicionalmente, las terapias para el Huntington han intentado reducir la producción de la proteína mutada o mitigar sus efectos tóxicos. Sin embargo, estos enfoques han tenido resultados limitados.
El nuevo trabajo propone un cambio de paradigma: atacar la propagación intercelular.
Si se consigue impedir que la proteína tóxica viaje de una neurona a otra, podría ralentizarse significativamente la progresión de la enfermedad neurodegenerativa. En ese contexto, Slc4a7 aparece como una diana terapéutica atractiva.
De hecho, los investigadores ya han probado inhibidores como el DIDS, que reducen tanto la formación de nanotúneles como el transporte de la proteína mutada . Aunque estos compuestos no están diseñados específicamente para uso clínico en este contexto, demuestran que el mecanismo es susceptible de intervención.
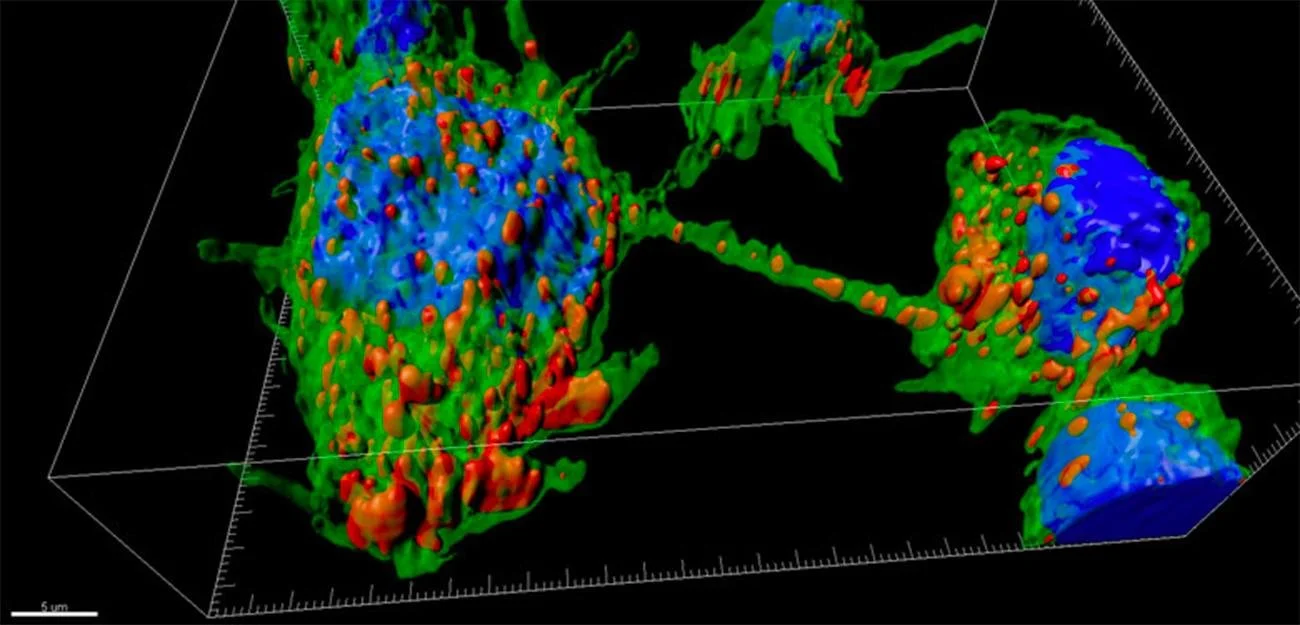
Células neuronales conectadas por nanotúneles (TNT) que permiten el paso de agregados proteicos (en rojo), un mecanismo similar al descrito en el estudio para la propagación de proteínas tóxicas en enfermedades neurodegenerativas como el Huntington. Cortesía: Institut Pasteur
Implicaciones más allá del Huntington
El impacto del descubrimiento podría ir más allá de esta enfermedad. Cada vez hay más evidencias de que proteínas mal plegadas en trastonos neurodegenerativos como el alzhéimer o el párkinson también se propagan entre células.
El estudio sugiere que los nanotubos podrían ser una vía común para esa transmisión, y que el eje Rhes-Slc4a7 podría desempeñar un papel más amplio en la neurodegeneración.
Además, estos mismos mecanismos podrían estar implicados en el cáncer, donde los nanotúneles facilitan la comunicación entre células tumorales y su entorno.
🗣️ «Esta investigación pone de relieve una forma completamente nueva en que las células se comunican en condiciones de salud y enfermedad —afirma Randy Blakely, director del Instituto Cerebral Stiles-Nicholson de la FAU y profesor de Neurociencia y de Ciencias Biomédicas en la Facultad de Medicina de la FAU. Y continúa—: Al comprender cómo las proteínas dañinas se desplazan físicamente de una célula a otra, obtenemos nuevos y potentes puntos de apoyo para el tratamiento. La idea de que podríamos ralentizar o incluso detener la progresión de la enfermedad bloqueando estos túneles microscópicos abre una frontera apasionante para el tratamiento no solo de la enfermedad de Huntington, sino también de una amplia gama de trastornos neurológicos y cánceres en el futuro».
Un cambio en la forma de entender la enfermedad
El trabajo de Dagar y sus colegas refuerza una idea que está transformando la neurología: las enfermedades neurodegenerativas no son solo procesos internos de cada célula, sino fenómenos de red.
Las neuronas no enferman de forma aislada. Se influyen, se comunican y, en algunos casos, se dañan mutuamente.
Los diminutos túneles descubiertos en este estudio son una prueba de ello. Invisibles al ojo humano, pero decisivos en la progresión de la enfermedad, representan tanto un problema como una oportunidad.
Porque, si la enfermedad se propaga, también puede detenerse.▪️(20-marzo-2026)
PREGUNTAS&RESPUESTAS: Huntington y nanotubos
🧠 ¿Qué es la enfermedad de Huntington?
Es una dolencia neurodegenerativa genética causada por una mutación que produce una proteína tóxica (huntingtina mutada) que daña las neuronas.
🧠 ¿Qué son los nanotubos celulares?
Son estructuras microscópicas que conectan células y permiten el intercambio directo de proteínas y otros componentes.
🧠 ¿Cómo se propaga la enfermedad de Huntington en el cerebro?
La proteína mutada puede transferirse entre neuronas a través de nanotúneles celulares, extendiendo el daño.
🧠 ¿Qué papel tienen las proteínas Rhes y Slc4a7?
Rhes promueve la formación de nanotúneles y Slc4a7 regula el entorno químico necesario para que se formen y funcionen.
🧠 ¿Se puede frenar la enfermedad bloqueando este mecanismo?
Sí. El estudio muestra que inhibir Slc4a7 reduce la propagación de la proteína tóxica, lo que podría ralentizar la enfermedad.
Información facilitada por la FAU
Fuente: Sunayana Dagar et al. Membrane-associated Rhes-Slc4a7 complex orchestrates tunneling nanotube formation and mutant Huntingtin spread. Science Advances (2026). DOI:10.1126/sciadv.aea1226