Proteínas cuánticas vivas: un equipo de Oxford diseña sensores biológicos basados en física cuántica
Por primera vez, la física cuántica deja de ser un fenómeno observado en la naturaleza para convertirse en una herramienta diseñada dentro de células vivas. Un equipo de la Universidad de Oxford ha creado proteínas fluorescentes capaces de actuar como sensores cuánticos, un avance que abre una nueva frontera en la biotecnología y la biomedicina.
Por Enrique Coperías, periodista científico
Ilustración conceptual de una proteína fluorescente magnetosensible diseñada por un equipo de la Universidad de Oxford, capaz de interactuar con campos magnéticos y ondas de radio mediante procesos cuánticos dentro de células vivas, un avance que abre nuevas aplicaciones en biotecnología y biomedicina. Crédito: IA-DALL-E-©RexMolón Producciones
Tradicionalmente, la física cuántica ha sido territorio casi exclusivo de laboratorios ultraespecializados, diamantes artificiales, sensores criogénicos y dispositivos alejados de la biología. Ahora, un equipo internacional liderado desde la Universidad de Oxford, en el Reino Unido, ha dado un paso de gigante que desdibuja esa frontera: ha conseguido diseñar proteínas vivas capaces de explotar fenómenos cuánticos medibles dentro de células, a temperatura ambiente y con herramientas estándares de la biología.
El avance, publicado en la revista Nature, no solo amplía el campo emergente de la biología cuántica, sino que inaugura una nueva generación de sensores biotecnológicos basados en principios cuánticos.
El trabajo demuestra que es posible crear proteínas fluorescentes, similares a las que ya se usan de forma rutinaria en biología, cuya emisión de luz cambia de forma controlable en presencia de campos magnéticos y ondas de radio.
Esos cambios no son un efecto químico trivial, sino la huella directa de un proceso cuántico: la dinámica de espines electrónicos —una propiedad cuántica de los electrones, similar a un pequeño imán interno, que determina cómo interactúan con campos magnéticos y entre sí— acoplados en lo que se conoce como un par radical. Este es estado transitorio en el que dos moléculas o átomos con electrones no apareados se crean al mismo tiempo y cuyos espines quedan correlacionados cuánticamente, lo que hace que su evolución sea sensible a campos magnéticos.
En otras palabras, estas proteínas funcionan como diminutos sensores cuánticos vivos.
¿Qué significa que una proteína tenga «capacidad cuántica»?
La idea de que la vida pueda apoyarse en fenómenos cuánticos no es nueva. Desde hace años, los científicos debaten sobre si algunas aves perciben el campo magnético terrestre gracias a reacciones cuánticas en unas proteínas fotorreceptoras llamadas criptocromos o si ciertos procesos fotosintéticos aprovechan las coherencias cuánticas —situaciones en las que partículas cuánticas existen simultáneamente en varios estados posibles, manteniendo una relación de fase ordenada que les permite comportarse de forma coordinada durante un breve tiempo— para optimizar la transferencia de energía.
Pero esos ejemplos han sido difíciles de estudiar, frágiles y, sobre todo, imposibles de convertir en herramientas prácticas. El avance de Oxford cambia radicalmente ese panorama.
El punto de partida del estudio es una familia de proteínas bautizadas como MagLOV, derivadas de un dominio fotosensible presente en las plantas. Estas proteínas contienen una molécula de flavina, un cofactor —una molécula auxiliar que una proteína o enzima necesita para funcionar correctamente y llevar a cabo una reacción biológica— común en biología, que al absorber luz inicia una cascada de reacciones electrónicas.
En ese proceso se forma un par de electrones no apareados cuyos espines quedan entrelazados durante un breve instante. Esa correlación cuántica determina si la reacción regresa al estado inicial o sigue otros caminos químicos, y lo hace de forma sensible a campos magnéticos externos.
Una sensibilidad que se puede ver
Lo extraordinario del trabajo es que los autores han demostrado que esa sensibilidad no solo existe, sino que puede leerse ópticamente. Al iluminar bacterias vivas que expresan proteínas MagLOV, la fluorescencia de la proteína disminuye o aumenta en función de si se aplica un campo magnético o una señal de radiofrecuencia concretos.
Esa respuesta, conocida como resonancia magnética detectada ópticamente (ODMR), se ha observado hasta ahora en materiales artificiales, pero rara vez en sistemas biológicos vivos, y nunca con esta claridad y estabilidad.
Más aún: la señal es lo bastante intensa como para poder ser detectada en células individuales. Es decir, una sola bacteria puede funcionar como un sensor cuántico autónomo, visible bajo un microscopio convencional. Según los autores, esta sensibilidad excepcional se debe a la combinación de detección óptica —mucho más eficiente que otros métodos— y a la alta polarización del espín que se genera de forma natural en el par radical de la proteína.
Gabriel Abrahams (izquierda) y Harrison Steel, investigadores de la Universidad de Oxford y autores de un estudio publicado en Nature que demuestra que es posible diseñar proteínas con comportamiento cuántico dentro de células vivas. Foto: Olivia Gaskin.
Proteínas mejoradas mediante evolución dirigida
Uno de los aspectos clave del estudio es que estas proteínas no se han descubierto tal cual en la naturaleza, sino que han sido mejoradas mediante evolución dirigida. El equipo introdujo mutaciones sistemáticas en el gen de partida y seleccionó las variantes que mostraban respuestas magnéticas más intensas o más rápidas. Así surgieron versiones especializadas de MagLOV, algunas optimizadas para maximizar el contraste de la señal y otras para responder con mayor rapidez a los cambios de campo.
🗣️ Para Gabriel Abrahams, primer autor del estudio y doctorando en el Departamento de Ingeniería de Oxford, el proceso encierra una lección fundamental: «Es un descubrimiento enormemente emocionante. Lo que más me asombra es el poder de la evolución: todavía no sabemos cómo diseñar desde cero un buen sensor cuántico biológico, pero al dirigir cuidadosamente el proceso evolutivo en bacterias, la naturaleza encontró una solución para nosotros».
Esta capacidad de ingeniería genética marca una diferencia crucial con otros sensores cuánticos. Mientras que los centros de vacante de nitrógeno en diamantes —uno de los sensores cuánticos más usados— requieren procesos de fabricación complejos y no pueden integrarse fácilmente en organismos vivos, las proteínas MagLOV se codifican en ADN, se expresan dentro de las células y pueden modificarse con técnicas estándar de biología molecular. La cuántica, por primera vez, entra en el toolkit habitual de la biotecnología.
Aplicaciones biomédicas y tecnológicas
Las aplicaciones potenciales son tan amplias como inesperadas. Una de las más inmediatas es la multiplexación en imagen biológica, la técnica que permite visualizar y distinguir varios procesos o moléculas diferentes al mismo tiempo en una muestra biológica. Hoy, el número de señales que pueden distinguirse simultáneamente en un experimento de fluorescencia está limitado por el color de los marcadores.
MagLOV introduce una nueva dimensión: dos proteínas del mismo color pueden diferenciarse por cómo responden al campo magnético o a la radiofrecuencia. Esto permitiría etiquetar más procesos celulares sin saturar el espectro óptico.
Otra aplicación destacada es la llamada detección lock-in, una técnica usada en física para extraer señales débiles del ruido. Al modular el campo magnético y observar solo la parte de la fluorescencia que oscila al mismo ritmo, los investigadores logran identificar proteínas MagLOV incluso cuando su brillo es bajo o cuando la muestra presenta autofluorescencia y dispersión de luz, problemas habituales en tejidos vivos.
Sensores que chequean el microambiente en las células
Quizá el resultado más sorprendente sea la demostración de una especie de resonancia magnética por fluorescencia. Como la frecuencia de resonancia de la proteína depende del campo magnético local, es posible usar gradientes magnéticos —similares a los de una resonancia magnética convencional (MRI)— para localizar la posición de células fluorescentes en un volumen tridimensional, incluso sin captar imágenes espaciales directas.
En el estudio, los autores construyeron un prototipo que permite localizar capas de bacterias dentro de un material opaco con una precisión del orden del milímetro.
Además, las proteínas muestran sensibilidad al entorno magnético microscópico. Cuando se añaden agentes paramagnéticos, como los usados en contraste de resonancia magnética clínica, la señal cuántica de MagLOV se atenúa de forma predecible. Esto sugiere que estas proteínas podrían actuar como sensores del microambiente celular, y detectar la presencia de radicales libres o metales paramagnéticos implicados en procesos fisiológicos y patológicos.
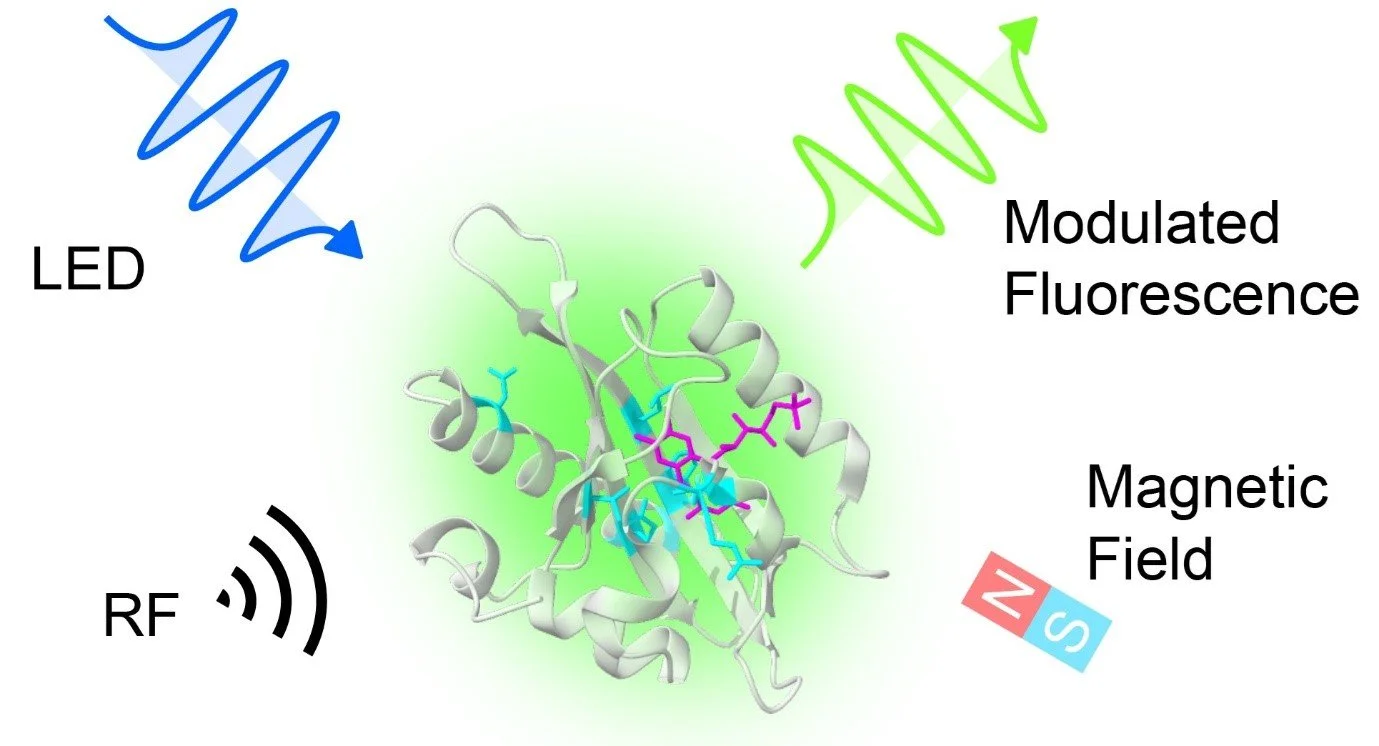
Las proteínas fluorescentes magnetosensibles (MFP) se activan con luz —en este caso, emitida por un LED azul— y responden emitiendo fluorescencia verde. La intensidad de esa luz puede modularse mediante la aplicación de campos magnéticos u ondas de radio, una propiedad basada en procesos cuánticos dentro de la proteína. Cortesía: Gabriel Abrahams.
El equivalente cuántico a lo que supuso la proteína verde fluorescente para la biología
En conjunto, el trabajo representa un cambio de paradigma. Por primera vez, un sistema biológico cuántico no solo se observa o se modela, sino que se diseña, se optimiza y se utiliza como herramienta.
🗣️ El autor sénior del estudio, Harrison Steel, profesor del Departamento de Ingeniería de Oxford, subraya que el camino hasta este resultado no ha sido lineal: «Nuestro estudio pone de relieve lo difícil que es predecir el camino sinuoso que lleva de la ciencia fundamental a un avance tecnológico. Por ejemplo, nuestra comprensión de los procesos cuánticos que tienen lugar dentro de las proteínas fluorescentes magnetosensibles o MFP solo fue posible gracias a expertos que han dedicado décadas a estudiar cómo se orientan las aves utilizando el campo magnético de la Tierra. Mientras tanto, las proteínas que sirvieron como punto de partida para diseñar las MFP procedían de algo tan común como la avena».
«Es el equivalente cuántico a lo que supuso la proteína verde fluorescente para la biología», señalan los autores en su artículo: un marcador que transformó la investigación al permitir ver procesos invisibles, y que ahora podría tener su contraparte cuántica.
Por qué este avance supone un cambio de paradigma
Quedan, por supuesto, muchos desafíos. Las proteínas MagLOV aún pueden mejorarse en brillo, estabilidad y sensibilidad. Su uso en organismos más complejos exigirá resolver problemas de entrega genética y control de campos magnéticos. Y el entendimiento detallado de los mecanismos cuánticos subyacentes sigue siendo un campo activo de investigación. Pero el camino está abierto.
Steel destaca también el papel del apoyo institucional y financiero para hacer posible este tipo de investigación híbrida: «Estamos inmensamente agradecidos a quienes han apoyado nuestro trabajo, en particular a la financiación del programa EEBio del EPSRC, que ha sido fundamental para hacer posible nuestra visión interdisciplinar de llevar a cabo bioingeniería junto con robótica, algoritmos de control e inteligencia artificial, todo en un mismo laboratorio».
La frontera entre física cuántica y biología, durante mucho tiempo conceptual y experimental, empieza a diluirse. En lugar de sensores fríos y artificiales, la cuántica se vuelve blanda, viva y programable. Si el siglo XX fue el de la física cuántica y el XXI el de la biología sintética, este trabajo sugiere que el próximo territorio fértil está justo en su intersección.▪️(22-enero-2026)