¿Puede una terapia regenerativa curar la parálisis? Un avance con organoides de médula espinal humana abre nuevas posibilidades
Una innovadora terapia experimental logra regenerar tejido nervioso y reducir la cicatrización en mini médulas espinales humanas cultivadas en laboratorio. El hallazgo refuerza la esperanza de futuros tratamientos capaces de revertir la parálisis tras una lesión medular, hoy por hoy, irreparable.
Por Enrique Coperías, periodista científico
Estas micrografías fluorescentes muestran un mayor crecimiento de neuritas en un organoide de médula espinal humana tratado con moléculas danzantes de movimiento rápido (izquierda) frente a otro tratado con moléculas más lentas con las mismas señales bioactivas (derecha). Cortesía: Samuel I. Stupp / Northwestern University
Un equipo de científicos de la Universidad Northwestern, en Estados Unidos, ha logrado reproducir en el laboratorio, con un nivel de detalle sin precedentes, las lesiones de la médula espinal humana y probar en ese modelo una terapia experimental que podría abrir la puerta a nuevos tratamientos contra la parálisis.
En España, la lesión medular sigue siendo un problema sanitario relevante, con una incidencia de unos treinta nuevos casos por millón de habitantes y más de 150.000 afectados. según el Hospital Nacional de Parapléjicos, en Toledo (España). Cada año se registran alrededor de mil nuevos casos traumáticos, aproximadamente la mitad por accidentes de tráfico y el resto por caídas, golpes, accidentes deportivos u otros traumatismos, como las zambullidas.
A estas cifras se suma cerca de un 30% adicional de lesiones de origen médico —por enfermedades como la esclerosis múltiple, tumores o infecciones vertebrales— y causas congénitas, caso del mielomeningocele. La mayoría de las parálisis se concentran en la población joven: el mayor número de lesiones se produce entre los dieciséis y treinta años, y cerca del 80% ocurre antes de los 45.
En la mayoría de los casos, la parálisis se debe a traumatismos vertebrales
Según el nivel de afectación, las lesiones pueden provocar tetraplejía —cuando la parálisis afecta a las cuatro extremidades— o paraplejía —si solo afecta a las inferiores—; y según su extensión pueden ser completas, cuando la médula queda totalmente dañada, o incompletas, cuando se conserva alguna conexión con el cerebro.
En la mayoría de los casos el daño se debe a traumatismos vertebrales que comprimen o desgarran la médula espinal, interrumpiendo la transmisión de señales entre el cerebro y el resto del cuerpo. Como consecuencia, por debajo de la lesión se pierden total o parcialmente las funciones motoras, sensitivas y autonómicas, mientras que la parte superior del cuerpo continúa funcionando con normalidad.
En este contexto de graves secuelas y escasas opciones terapéuticas efectivas, la investigación científica busca desde hace años estrategias capaces de regenerar el tejido nervioso dañado y restaurar las conexiones perdidas.
El estudio, que se ha publicado en la revista Nature Biomedical Engineering, describe cómo una tecnología basada en las llamadas moléculas danzantes estimula el crecimiento neuronal y reduce la cicatrización en organoides de médula espinal humana lesionados.
La paraplejía se produce cuando una lesión medular en la zona dorsal, lumbar o sacra provoca la pérdida de sensibilidad y de movimiento en la parte inferior del cuerpo. Imagen de Francisco Zuasti en Pixabay
Qué son los organoides de médula espinal y por qué son clave para estudiar la parálisis
Los organoides, pequeños tejidos tridimensionales cultivados a partir de células madre que emulan la microanatomía, la estructura y las funciones de los órganos humanos. Actúan como miniórganos (cerebro, pulmón, tumoroides, hígado) y son cada vez más utilizados en la investigación biomédica para estudiar enfermedades, probar fármacos personalizados y reducir la experimentación animal.
En este caso, el equipo ha desarrollado el modelo de organoide de médula espinal humana más avanzado hasta la fecha para estudiar lesiones traumáticas y evaluar posibles terapias regenerativas.
Por primera vez, los investigadores han demostrado que estos organoides pueden reproducir con precisión los efectos fundamentales de una lesión medular: muerte celular, inflamación y la formación de cicatrices gliales, un tejido denso que actúa como barrera física y química para la regeneración nerviosa. Cuando aplicaron la nueva terapia, observaron un crecimiento significativo de neuritas —las prolongaciones de las neuronas que permiten la comunicación entre células, como axones y dendritas— y una reducción notable de ese tejido cicatricial.
🗣️«Uno de los aspectos más emocionantes de los organoides es que podemos usarlos para probar nuevas terapias en tejido humano —explica Samuel I. Stupp, autor principal del estudio e inventor de las moléculas danzantes— . Y añade—: A falta de un ensayo clínico, es la única manera de lograr este objetivo. Decidimos desarrollar dos modelos distintos de lesión en un organoide de médula espinal humana y probar nuestra terapia para ver si los resultados se parecían a lo que habíamos observado previamente en el modelo animal».
En palabras de este ingeniero biomédico, «tras aplicar la terapia, la cicatriz glial se redujo significativamente hasta volverse apenas detectable, y vimos crecer neuritas, semejando la regeneración de axones que observamos en animales. Esto valida que nuestra terapia tiene muchas posibilidades de funcionar en humanos».
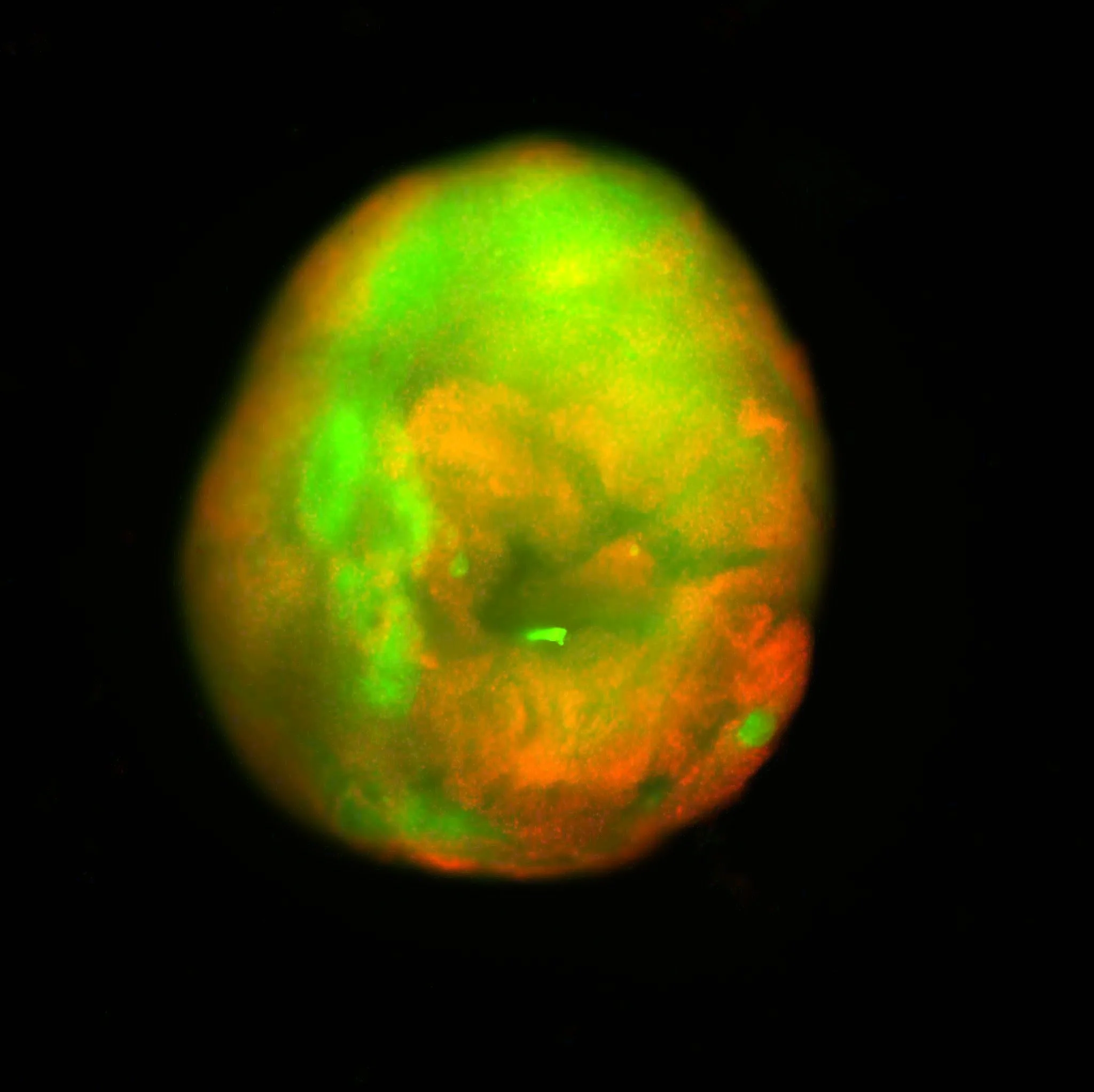
Imagen fluorescente de un organoide humano de médula espinal con lesión por contusión: las células muertas aparecen en rojo y las vivas en verde. Cortesía: Samuel I. Stupp / Northwestern University.
Un modelo de lesión medular más realista que nunca
Cultivados a partir de células madre pluripotentes inducidas (iPSC) —células adultas reprogramadas genéticamente para comportarse como células madre embrionarias—, los organoides son versiones simplificadas de órganos humanos reales. Aunque incompletos, imitan la estructura tisular, la complejidad celular y parte de la función del órgano original.
Esa capacidad de imitación los convierte, como ya se ha mencionado, en modelos idóneos para estudiar enfermedades, probar tratamientos y comprender el desarrollo de los tejidos. Además, las pruebas en organoides son más rápidas y mucho menos costosas que en animales o personas.
En el caso de la médula espinal, ya existían organoides para estudiar aspectos fisiológicos básicos, pero el modelo desarrollado por el equipo de la Northwestern representa un salto importante para investigar lesiones paralizantes. Con varios milímetros de diámetro, estos organoides son lo bastante grandes y maduros como para reproducir daños reales.
Stupp y su equipo los cultivó durante meses hasta que desarrollaron características complejas, incluidas neuronas y astrocitos. También añadieron microglía —células inmunitarias del sistema nervioso central— para simular la respuesta inflamatoria tras una lesión traumática.
🗣️ «Es una especie de pseudoórgano —afirma Stupp. Y comenta—: Fuimos los primeros en introducir microglía en un organoide de médula espinal humana, así que fue un logro enorme. Significa que nuestro organoide tiene todos los compuestos químicos que el sistema inmunitario residente produce en respuesta a una lesión. Eso lo convierte en un modelo de lesión medular más realista y preciso».
Qué son las «moléculas danzantes» y cómo podrían revertir la parálisis
Una vez desarrollado el organoide, el equipo simuló distintos tipos de lesiones medulares: algunas mediante cortes con bisturí, semejantes a heridas quirúrgicas, y otras por compresión, como las que pueden producirse en accidentes de tráfico o caídas. Ambos tipos de daño provocaron muerte celular y formación de cicatrices gliales, tal como ocurre en una lesión real.
«Podíamos distinguir entre los astrocitos que forman parte del tejido normal y los astrocitos de la cicatriz glial, que son grandes y están muy densamente empaquetados —explica Stupp en un comunicado de la Northwestern—. También detectamos la producción de proteoglicanos de sulfato de condroitina, moléculas del sistema nervioso que responden a la lesión y a la enfermedad».
Tras provocar las lesiones, los investigadores aplicaron la terapia de moléculas danzantes, presentada por primera vez en 2021. Se trata de una plataforma de péptidos terapéuticos supramoleculares diseñada para activar receptores celulares mediante señales naturales del organismo y promover la regeneración. Inyectada en forma líquida, la terapia se transforma rápidamente en un gel compuesto por nanofibras que imitan la matriz extracelular de la médula espina, la estructura del sistema nervioso central que recorre el interior de la columna vertebral y actúa como vía de comunicación entre el cerebro y el resto del cuerpo, transmitiendo las señales que permiten el movimiento, la sensibilidad y funciones automáticas como la respiración o el control de órganos.
La clave reside en el movimiento colectivo de las moléculas dentro de esas nanofibras. Ajustando esa danza, el equipo comprobó que la terapia se conecta con mayor eficacia a los receptores celulares, que también están en constante movimiento.
«Dado que las propias células y sus receptores están en constante movimiento, se puede imaginar que las moléculas que se mueven más rápido se encontrarán con esos receptores con mayor frecuencia —explicaba Stupp en 2021—. Si las moléculas son lentas y no tan ‘sociales’, puede que nunca entren en contacto con las células».
En estudios previos con animales, una sola inyección administrada veinticuatro horas después de una lesión grave permitió a ratones recuperar la capacidad de caminar en cuatro semanas. Las formulaciones con mayor movilidad molecular mostraron una eficacia terapéutica superior.
Resultados: crecimiento de neuritas y reducción de la cicatriz glial
En los organoides lesionados, la terapia formó un andamiaje que redujo la inflamación, disminuyó la cicatriz glial, estimuló la extensión de neuritas y favoreció que las neuronas crecieran en patrones ordenados.
La regeneración de neuritas —especialmente de los axones, que suelen romperse tras una lesión medular— podría restablecer las conexiones neuronales y evitar o revertir la parálisis y la pérdida de sensibilidad.
Stupp atribuye el éxito del tratamiento a ese movimiento supramolecular: «antes incluso de desarrollar el modelo de lesión, probamos la terapia en un organoide sano. Las moléculas danzantes hicieron brotar todas estas largas neuritas en la superficie del organoide pero, cuando utilizamos moléculas con menos o ningún movimiento, no vimos nada. La diferencia fue muy clara».
Próximos pasos: medicina personalizada y ensayos en humanos
Los investigadores planean ahora desarrollar organoides aún más complejos para perfeccionar el modelo y estudiar lesiones crónicas, que suelen presentar cicatrices más resistentes.
A largo plazo, los organoides de médula espinal también podrían utilizarse en medicina personalizada, creando tejido implantable a partir de las propias células madre del paciente para evitar el rechazo inmunitario.
Aunque el camino hasta la aplicación clínica es largo, el estudio ofrece una validación clave en tejido humano. Y, por primera vez, sugiere que una terapia capaz de revertir la parálisis en animales podría tener también posibilidades reales en personas.▪️(11-febrero-2026)
TAMBIÉN TE PUEDE INTERESAR:
🦽Una tecnología pionera ayuda a un hombre con ELA a «hablar» en tiempo real
🦽Un implante cerebral permite a un hombre con parálisis pilotar un dron virtual con el pensamiento
🦽Andamios impresos en 3D para lesiones de médula espinal: el avance que podría devolver la movilidad
🦽La estimulación del hipotálamo devuelve la marcha a dos pacientes con lesión medular
Información facilitada por la Universidad Northwestern
Fuente: Takata, N., Li, Z., Metlushko, A. et al. Injury and therapy in a human spinal cord organoid. Nature Biomedical Engineering (2026). DOI: https://doi.org/10.1038/s41551-025-01606-2