Un trasplante de células madre editadas genéticamente abre una nueva vía contra las leucemias más agresivas
Una técnica basada en la edición genética CRISPR logra proteger la médula ósea sana mientras una inmunoterapia ataca las células tumorales en pacientes con leucemia mieloide aguda. El avance podría allanar el camino hacia una nueva generación de terapias CAR-T contra cánceres de la sangre hasta ahora muy difíciles de tratar.
Por Enrique Coperías, periodista científico
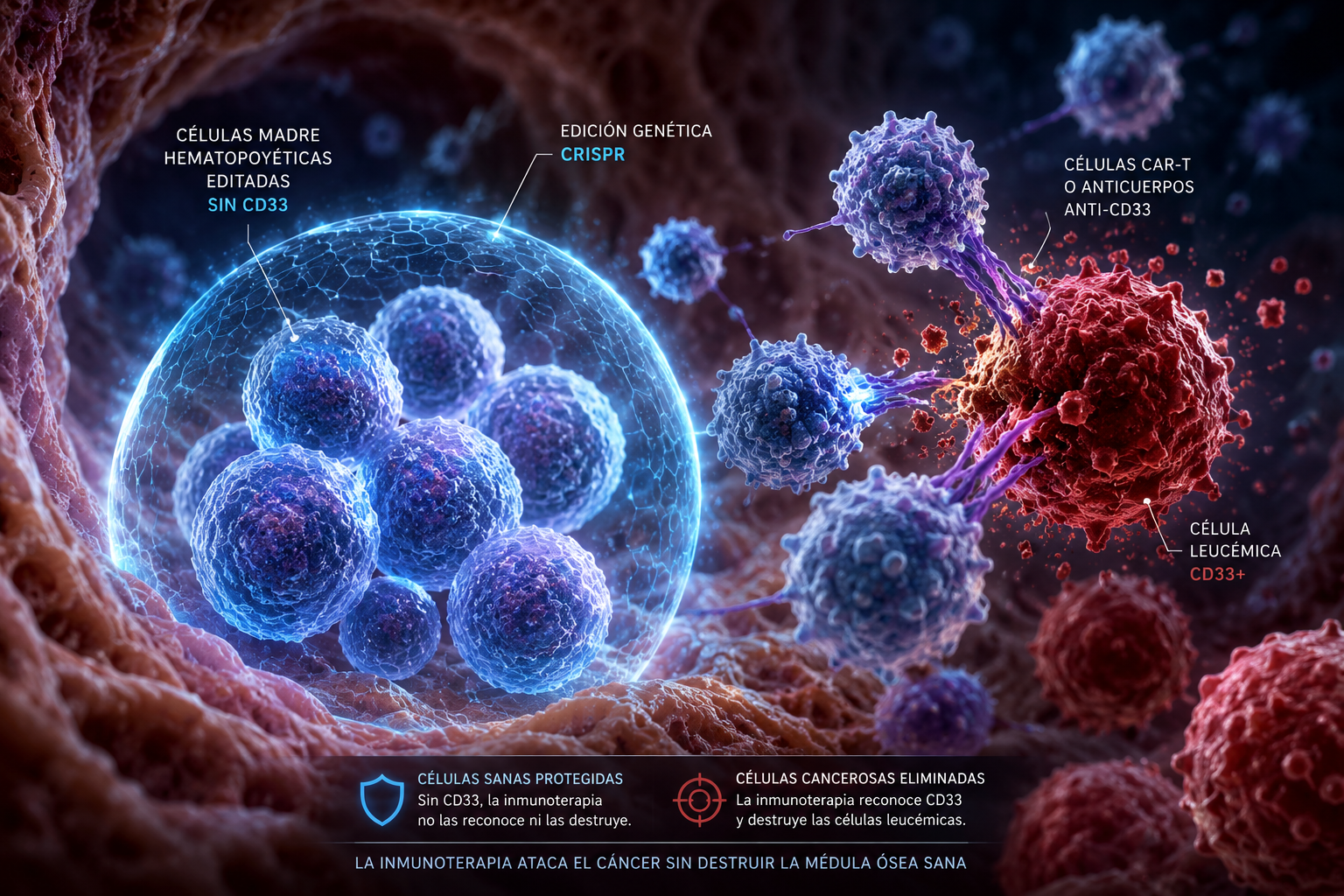
La ilustración muestra cómo las células madre hematopoyéticas editadas con CRISPR y privadas de la proteína CD33 pueden quedar protegidas frente a inmunoterapias dirigidas contra la leucemia, permitiendo atacar las células tumorales sin destruir la médula ósea sana. Crédito: IA-DALL-E-RexMolón Producciones
La medicina del cáncer lleva años persiguiendo una idea casi utópica: destruir las células tumorales sin arrasar al mismo tiempo las sanas. En los cánceres de la sangre, ese objetivo resulta especialmente difícil.
Esto es así porque las leucemias y otros tumores hematológicos comparten muchas de sus señas de identidad con las células normales de la médula ósea, de modo que cualquier tratamiento dirigido contra el tumor suele golpear también al sistema sanguíneo sano.
Ahora, un ensayo clínico liderado por investigadores de la Universidad Washington de Saint Louis y realizado en quince hospitales de Estados Unidos y Canadá, propone una estrategia que parece salida de la ciencia ficción: modificar genéticamente las células madre de un donante para hacerlas invisibles a una inmunoterapia y permitir así atacar el cáncer sin destruir la médula ósea trasplantada.
Qué han logrado los científicos
El estudio, que fue realizado en pacientes con leucemia mieloide aguda (LMA) y síndromes mielodisplásicos de alto riesgo, arroja unos resultados preliminares prometedores, según detallan sus autores en la revista Nature Medicine. Pero ¿cómo lo consiguieron?
Los investigadores utilizaron la tijera molecular CRISPR-Cas9 —la revolucionaria herramienta de edición genética desarrollada por las premio nobel Emmanuelle Charpentier y Jennifer A. Doudna— para eliminar un marcador llamado CD33 de las células madre hematopoyéticas del donante antes del implante. Recordemos que estas últimas son células primitivas de la médula ósea capaces de generar todos los tipos de células de la sangre, como los glóbulos rojos, los glóbulos blancos y las plaquetas.
Después administraron a los pacientes gemtuzumab ozogamicina, un fármaco dirigido precisamente contra el CD33. El resultado fue que las células tumorales seguían siendo vulnerables al tratamiento, pero las nuevas células sanguíneas sanas quedaban protegidas.
Por qué la leucemia mieloide aguda es tan difícil de tratar
La idea responde a uno de los mayores problemas de la leucemia mieloide aguda, el tipo de leucemia más común en la población adulta y que afecta cada año a más de 6.000 personas en España. Aunque muchos pacientes logran inicialmente una remisión, el riesgo de recaída sigue siendo muy elevado, incluso después de un trasplante alogénico de médula ósea, considerado la opción más agresiva y potencialmente curativa.
En los pacientes de alto riesgo —aquellos con mutaciones adversas, enfermedad residual detectable o recaídas previas— el pronóstico continúa siendo sombrío.
🗣️ «Esta tecnología de edición genética podría ayudar a resolver una frustración histórica del campo: las terapias CAR-T, eficaces frente a algunos cánceres hematológicos agresivos, no han funcionado bien contra enfermedades como la leucemia mieloide aguda y los síndromes mielodisplásicos», señala John F. DiPersio, hematólogo de la Universidad Washington en Saint Louis y principal autor del trabajo.
No hay que olvidar que la terapia con células CAR-T o terapia de linfocitos T con receptor de antígeno quimérico (CAR-T, por sus siglas en inglés) son un tipo de inmunoterapia personalizada en la que se extraen linfocitos T del propio paciente y se modifican genéticamente en laboratorio para que reconozcan y destruyan células cancerosas. Estos tratamientos han revolucionado algunos cánceres de la sangre, como ciertos linfomas y leucemias, pero su eficacia en tumores mieloides ha sido mucho más limitada debido a la dificultad de distinguir entre células tumorales y células sanguíneas sanas.
Qué es CD33 y por qué es importante
«La recaída después del trasplante es uno de los grandes desafíos clínicos», explican los autores del trabajo. El problema está en que las terapias de mantenimiento capaces de eliminar las células tumorales residuales suelen provocar toxicidades hematológicas graves. El sistema inmune recién reconstruido tras el trasplante queda extremadamente vulnerable.
La proteína CD33, que de forma natural participa en la señalización, la adhesión y la multiplicación celular, es una de las dianas más estudiadas en la leucemia mieloide aguda, porque aparece en la mayoría de las células leucémicas. Pero existe un inconveniente fundamental: también está presente en las células normales de la médula ósea, el tejido esponjoso situado en el interior de los huesos (pelvis, esternón, costillas, cráneo) que actúa como la fábrica principal de las células madre de la sangre. Eso significa que cualquier tratamiento contra CD33 actúa como una bomba de racimo biológica: destruye células cancerosas, sí, pero también gran parte de la producción normal de sangre.
🗣️ «Los cánceres mieloides son difíciles de tratar con CAR-T porque las proteínas que identifican a las células tumorales también están presentes en células sanguíneas sanas, incluidas las células madre trasplantadas —insiste DiPersio—. Por ello, la inmunoterapia puede destruir también tejido sano y desencadenar toxicidades graves».
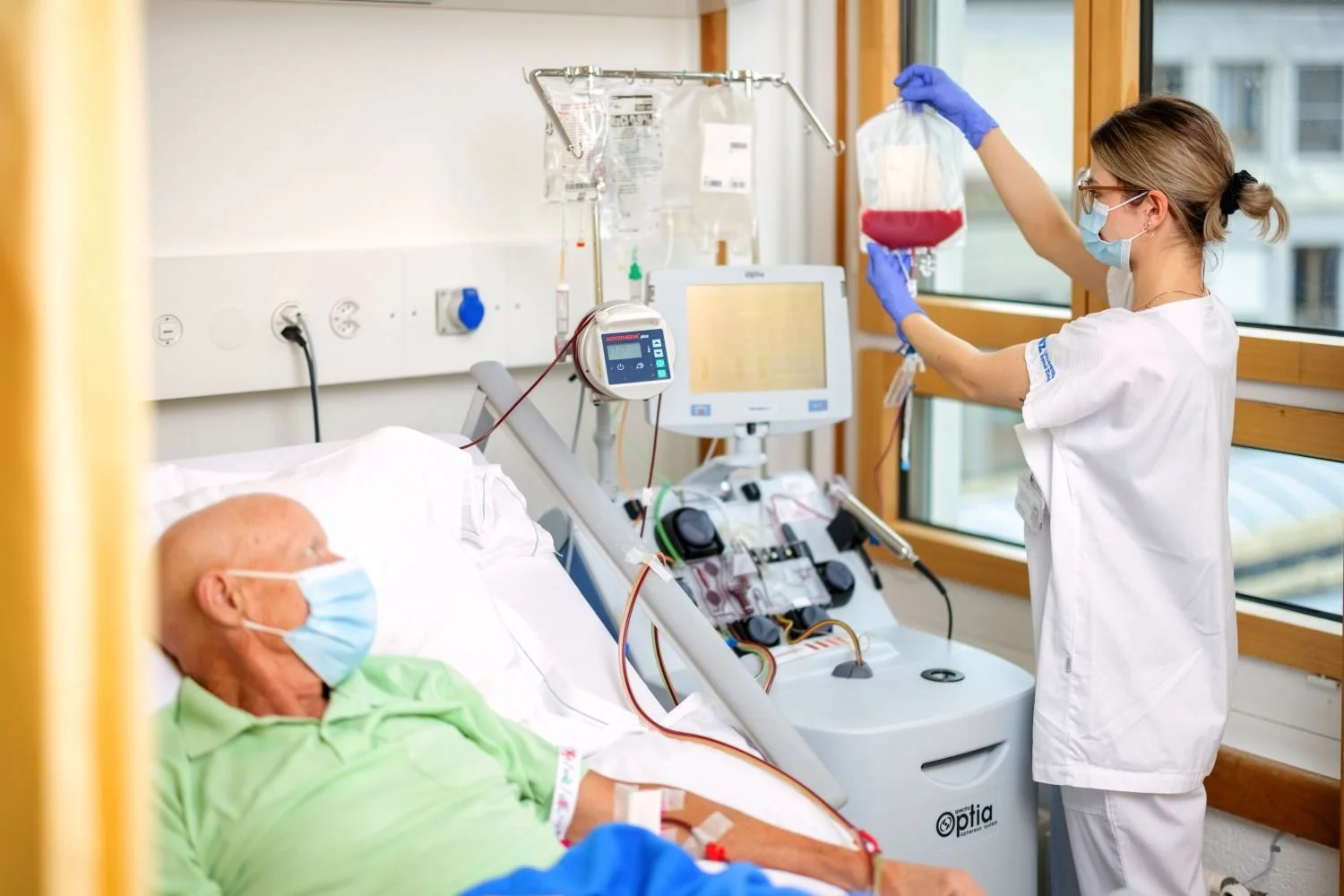
Un paciente recibe un procedimiento de extracción o trasplante de células madre hematopoyéticas, una terapia fundamental en el tratamiento de leucemias y otros cánceres de la sangre. Cortesía: University Hospital Zürich
Cómo funciona el trasplante de células madre editadas con CRISPR
La estrategia diseñada por el equipo internacional rompe esa limitación con una maniobra elegante:
1️⃣ Los científicos obtienen células madre hematopoyéticas del donante compatible.
2️⃣ En laboratorio, los investigadores utilizan la CRISPR-Cas9 para apagar el gen que dirige la síntesis de la proteína CD33.
3️⃣ El producto final, llamado tremtelectogene empogeditemcel otrem-cel, se infunde después del acondicionamiento intensivo previo al trasplante.
Una vez que las nuevas células sanguíneas editadas colonizan la médula ósea del paciente, los médicos pueden administrar gemtuzumab ozogamicina, un anticuerpo monoclonal humanizado que stá unido al citotóxico N‑acetil-gamma-calicheamicina. Como las células sanas trasplantadas ya no expresan CD33, el medicamento actúa sobre las células leucémicas restantes mientras deja relativamente intacto el nuevo sistema hematopoyético.
Resultados del ensayo clínico
El ensayo incluyó a treinta pacientes adultos con leucemia mieloide aguda o síndrome mielodisplásico de muy alto riesgo. Todos recibieron el trasplante con células editadas, y diecinueve de ellos recibieron posteriormente la inmunoterapia dirigida contra CD33.
Los resultados de seguridad fueron, al menos en esta fase inicial, muy prometedores. Los treinta pacientes lograron que las células madre trasplantadas prendieran correctamente en la médula ósea antes del vigesimoctavo día. Además, la recuperación de los neutrófilos —un tipo de glóbulo blanco fundamental para combatir infecciones— se produjo en una mediana de solo diez días.
🗣️ «Nos sentimos alentados por los resultados de este estudio, que muestran que un trasplante de células madre con deleción de CD33 presenta resultados muy similares a los de un trasplante estándar de células madre —afirma DiPersio. Y continúa—: En el futuro, esperamos poder combinar este enfoque con inmunoterapias dirigidas contra la CD33, como las células CAR-T, y mejorar las opciones de tratamiento para pacientes con estos cánceres sanguíneos tan agresivos».
Qué ventajas podría tener esta tecnología
Para los especialistas en trasplante, estos datos son importantes. Significan que la edición genética no pareció comprometer la capacidad de las células madre para regenerar la sangre. Una preocupación lógica de DiPersio y su equipo era que eliminar la CD33 pudiera alterar funciones esenciales de la hematopoyesis. Sin embargo, el estudio sugiere que las células editadas funcionan con relativa normalidad.
Los investigadores observaron además que las células modificadas persistían en distintas líneas sanguíneas —mieloides, linfocitos B y Natural Killer (NK)— sin mostrar desventajas aparentes frente a las células no editadas. También comprobaron que los neutrófilos conservaban funciones básicas, como la capacidad de producir estallidos oxidativos para destruir patógenos.
➡️ Uno de los aspectos más interesantes del trabajo es que proporciona una prueba de concepto de algo mucho más amplio que este tratamiento concreto. En realidad, la investigación apunta hacia una nueva filosofía terapéutica: reescribir genéticamente tejidos sanos para hacer posible inmunoterapias antes demasiado tóxicas.
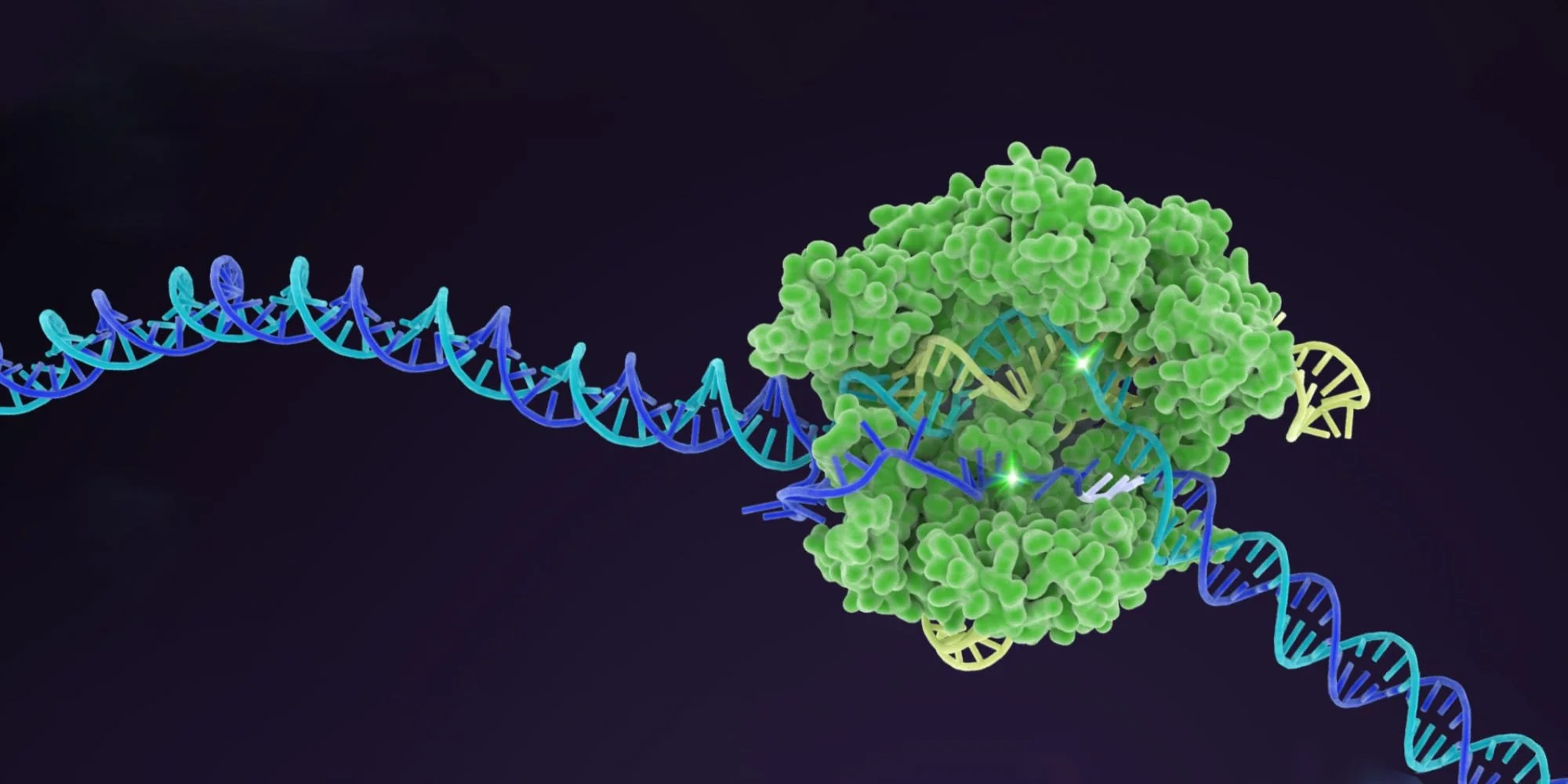
Ilustración de la herramienta de edición genética CRISPR-Cas9, una tecnología capaz de modificar fragmentos concretos de ADN y que está revolucionando la investigación biomédica y las terapias contra el cáncer. Cortesía: Innovative Genomics Institute
Convertir una diana «compartida» en una diana específica del cáncer
Durante años, las terapias celulares y los anticuerpos dirigidos contra cánceres hematológicos han tropezado con el mismo muro: las dianas tumorales suelen existir también en tejidos normales.
La posibilidad de blindar previamente esos tejidos sanos mediante edición genética abre escenarios completamente nuevos.
En este caso, la protección parece haber funcionado. Los pacientes tratados con gemtuzumab ozogamicina no desarrollaron las citopenias prolongadas que históricamente han limitado el uso de este fármaco tras un trasplante. Los recuentos de neutrófilos y plaquetas se mantuvieron relativamente estables incluso durante varios ciclos de tratamiento.
Riesgos y limitaciones del estudio
Eso no significa que el procedimiento sea inocuo. Hubo efectos adversos graves, que incluyeen infecciones graves, trombocitopenias —recuento bajo de plaquetas (trombocitos) en la sangre, lo que puede provocar sangrados anormales— y tres muertes relacionadas con el trasplante o sus complicaciones. Un paciente desarrolló síndrome de obstrucción sinusoidal hepática, una toxicidad conocida de la gemtuzumab ozogamicina.
Además, el ensayo era pequeño y estaba diseñado en esencia para evaluar la seguridad, no su eficacia definitiva. El seguimiento todavía es relativamente corto: la mediana fue de 7,9 meses. Aun así, los datos preliminares de supervivencia libre de recaída resultan alentadores para una población con pronóstico especialmente malo.
El estudio también aporta pistas biológicas interesantes sobre la evolución del cáncer. Todos los casos de recaída siguieron expresando la CD33. Esto sugiere que el tumor no escapó perdiendo la diana terapéutica, uno de los mecanismos clásicos de resistencia en inmunoterapia. Los investigadores creen que futuras generaciones de tratamientos anti-CD33 —como la CAR-T o los anticuerpos más sofisticados— podrían aprovechar todavía mejor esta plataforma de protección genética.
Por qué este estudio puede cambiar el futuro del «cortapega» genético
Más allá de la leucemia mieloide aguda, el trabajo se inserta en una tendencia creciente: utilizar el cortapega genético CRISPR no solo para corregir genes defectuosos, sino para rediseñar las reglas biológicas de los tratamientos oncológicos. Hasta hace pocos años, la edición genética clínica se concebía sobre todo como una herramienta para enfermedades hereditarias. Ahora empieza a utilizarse como una tecnología habilitadora para nuevas terapias del cáncer.
La lógica es poderosa. En lugar de limitar la potencia de una inmunoterapia para evitar daños colaterales, se modifica primero el organismo para hacerlo resistente al tratamiento. Algunos investigadores comparan esta estrategia con reforzar un edificio antes de utilizar explosivos para derribar una estructura vecina.
No obstante, el camino hacia una aplicación amplia todavía es largo. Los trasplantes alogénicos ya son procedimientos extremadamente complejos y caros. Añadir una fase de edición genética sofisticada multiplica la dificultad logística y regulatoria. Además, siguen existiendo interrogantes sobre los posibles efectos a largo plazo de la tecnología CRISPR en las células madre humanas.
Ilustración de células sanguíneas y leucocitos utilizada para representar el nuevo enfoque de trasplante de células madre editadas genéticamente, una estrategia que podría reducir la toxicidad y mejorar la eficacia de las terapias contra cánceres de la sangre. Cortesía: Sara Moser-WashU Medicine
Su elevado coste económico
Aunque la tecnología de edición ha mejorado enormemente, persiste la preocupación por alteraciones genéticas no deseadas o por cambios que solo se manifiesten años después.
En este ensayo no aparecieron señales claras de toxicidad genética inesperada, pero el número de pacientes y el tiempo de seguimiento son aún insuficientes para extraer conclusiones definitivas.
También queda por resolver una cuestión económica y ética de fondo: quién podrá acceder a este tipo de terapias ultracomplejas. Las inmunoterapias celulares actuales ya cuestan cientos de miles de euros por paciente. Incorporar ingeniería genética avanzada sobre células madre podría convertir estos tratamientos en algunos de los más caros de la historia de la medicina.
Qué significa este avance para los pacientes con leucemia
Pese a todas las cautelas, muchos expertos consideran que el estudio marca un momento importante. No tanto por los resultados clínicos inmediatos como por la demostración conceptual. Por primera vez, un ensayo clínico muestra que es posible editar genéticamente un injerto hematopoyético para protegerlo deliberadamente de una inmunoterapia posterior.
La propia conclusión de los autores resume la magnitud potencial del hallazgo: el trasplante con trem-cel «transforma la CD33 de un antígeno presente en toda la línea mieloide a una diana específica de la leucemia». En otras palabras, mediante ingeniería genética, los investigadores han conseguido redefinir qué pertenece al cáncer y qué pertenece al organismo sano.
«Los resultados del estudio sientan las bases para desarrollar intervenciones combinadas de trasplante de células madre con deleción de la CD33 e inmunoterapias dirigidas contra la CD33, evitando la destrucción de células sanas del donante durante el tratamiento del cáncer», concluye DiPersio.
Es una idea profundamente nueva. Y si funciona a gran escala, podría cambiar la manera en que se diseñan las inmunoterapias del futuro.▪️(13-mayo-2026)
PREGUNTAS&RESPUESTAS: Leucemia y CRISPR-Cas9
🧬 ¿Qué es la leucemia mieloide aguda?
La leucemia mieloide aguda es un cáncer agresivo de la sangre y la médula ósea caracterizado por la proliferación rápida de células sanguíneas anormales.
🧬 ¿Qué es CRISPR-Cas9?
CRISPR-Cas9 es una tecnología de edición genética, conocida popularmente como cortapega genético, que permite modificar ADN de forma precisa eliminando, corrigiendo o sustituyendo genes específicos.
🧬 ¿Qué es CD33?
CD33 es una proteína presente en la mayoría de las células de leucemia mieloide aguda y también en células normales de la médula ósea.
🧬 ¿Qué son las terapias CAR-T?
Las terapias CAR-T son inmunoterapias avanzadas que modifican linfocitos T para que reconozcan y destruyan células tumorales.
🧬 ¿Qué es trem-cel?
Trem-cel es un producto experimental de trasplante de células madre editadas genéticamente para eliminar la proteína CD33 antes del trasplante.
🧬 ¿El tratamiento ya está aprobado?
No. Se trata todavía de una terapia experimental evaluada en un ensayo clínico de fase 1/2.
SALUD Y MEDICINA
Información facilitada por la WashU Medicine
Fuente: DiPersio, J. F., Koehne, G., Shah, N. N. et al.CRISPR−Cas9 CD33-deleted allogeneic hematopoietic cell transplantation with gemtuzumab ozogamicin maintenance in AML: a phase 1/2 trial. Nature Medicine (2026). DOI: https://doi.org/10.1038/s41591-026-04362-1