BioConNet: la «placa de circuito» neuronal que imita las condiciones del cerebro humano en el laboratorio
Un equipo de neurocientíficos ha desarrollado una plataforma de bioingeniería capaz de recrear circuitos neuronales humanos con precisión arquitectónica y control funcional. El sistema, abierto y programable, permite estudiar cómo se conectan —y se desconectan— las neuronas en enfermedades como el alzhéimer y la ELA.
Por Enrique Coperías, periodista científico
Recreación artística y futurista de BioConNet en un laboratorio de neuroingeniería: una investigadora observa la plataforma bioingenierizada donde neuronas humanas se organizan en circuitos controlados y funcionales. Crédito: IA-DALL-E-RexMolón Producciones
Un avance en neuroingeniería para estudiar enfermedades neurodegenerativas
El cerebro humano no es una masa uniforme de neuronas que disparan impulsos eléctricos al azar. Estamos ante una arquitectura precisa, organizada en circuitos neuronales donde cada célula conecta con otras en patrones altamente específicos. Entender cómo se forman esos circuitos —y cómo se deterioran en enfermedades neurodegenerativas, como el alzhéimer, el párkinson y la esclerosis lateral amiotrófica (ELA), es uno de los grandes retos de la neurociencia contemporánea.
Un equipo internacional liderado desde el King’s College de Londres, en el Reino Unido, ha desarrollado ahora una plataforma de bioingeniería que permite construir en el laboratorio circuitos corticales humanos con una organización controlada y accesible. El sistema, descrito enl revista Advanced Healthcare Materials, funciona como una especie de placa de circuito neuronal abierta: una superficie microestructurada donde las neuronas crecen, se organizan en nodos definidos y establecen conexiones sinápticas en lugares predeterminados.
El avance no es menor. Hasta ahora, los modelos celulares del cerebro humano tenían un problema estructural: eran demasiado simples o demasiado complejos.
El dilema de los modelos neuronales
Desde 2007, cuando el japonés Shinya Yamanaka, Premio Nobel de Fisiología y Medicina en 2012 junto al biólogo británico John Gurdon, logró reprogramar células adultas en células madre pluripotentes inducidas (iPSC), los laboratorios pueden generar neuronas humanas a partir de células de la piel de un paciente. Esta tecnología ha revolucionado el estudio de enfermedades neurológicas, al permitir observar procesos celulares humanos que no pueden replicarse fielmente en modelos animales.
Sin embargo, cultivar neuronas en una placa bidimensional tradicional implica aceptar una limitación: las células crecen en orientaciones aleatorias y establecen conexiones sin una organización espacial definida. El resultado es una red funcional, pero desordenada. Eso dificulta estudiar fenómenos dependientes de la arquitectura del circuito, como la direccionalidad de las conexiones y la competencia sináptica, el proceso por el cual varias neuronas compiten entre sí para establecer o mantener conexiones con una misma neurona.
En el extremo opuesto están los organoides cerebrales, pequeñas estructuras tridimensionales que imitan parcialmente el desarrollo embrionario del cerebro. Son más complejos, pero también menos accesibles: resulta difícil manipular su actividad eléctrica con precisión, aislar regiones concretas o recuperar material celular para análisis moleculares.
Tecnología BioConNet: neuronas rojas y verdes cultivadas establecen conexiones entre sí; en la imagen ampliada, la línea blanca indica una escala de 200 μm. Cortesía: King's College London
Cómo funciona BioConNet: ingeniería de circuitos neuronales humanos
1️⃣ Microtopografía guiada con polímeros biocompatibles
El nuevo sistema, bautizado como BIOCONNET (Bioengineered Cortical Neuronal Network), busca situarse en un punto intermedio: combinar la accesibilidad de los cultivos 2D con la relevancia estructural de los modelos tridimensionales .
🗣️ «Podemos adaptar estos circuitos para experimentos individuales y para comprender enfermedades específicas. Esto nos permitirá entender tanto los mecanismos que hay detrás de la muerte celular en las enfermedades neurodegenerativas como probar nuevas terapias potenciales», explica la autora sénior del trabajo, el doctor Andrea Serio.
2️⃣ Microtopografía guiada con polímeros biocompatibles
La clave del dispositivo está en su diseño físico. Los investigadores fabricaron una superficie de polidimetilsiloxano (PDMS) —un polímero habitual en bioingeniería— con microcanales de apenas 10 micrómetros de ancho y alto. Estas microestrías actúan como guías físicas que orientan el crecimiento de las prolongaciones neuronales: los axones, que envían la señal eléctrica hacia otras célula; y las dendritas, que reciben las señales de otras neuronas.
Sobre esa superficie colocan, temporalmente, una guía de siembra: una estructura que delimita dónde se depositan las células. Tras 48 horas, la guía se retira, dejando un sistema completamente abierto, sin compartimentos cerrados ni barreras físicas permanentes.
3️⃣ Formación de nodos neuronales estables
Las neuronas derivadas de iPSC no se distribuyen de manera uniforme: tienden a autoorganizarse en pequeños grupos. El equipo aprovechó esta propiedad natural y ajustó el número de células sembradas hasta identificar un umbral crítico. Solo a partir de una densidad equivalente a 8–16 capas teóricas de empaquetamiento hexagonal se formaba un único nodo neuronal compacto y coherente .
🗣️ «Descubrimos cómo mantener estos nodos neuronales como una única unidad estable dentro de un circuito, algo que solo ocurre cuando el número de células y el tiempo son exactamente los adecuados. De lo contrario, las neuronas formaban múltiples grupos separados y no conseguían conectarse de manera consistente”, explica la primera autora del estudio, la doctora Pacharaporn Suklai.
Estos nodos funcionan como unidades dentro del circuito: conjuntos de neuronas que reciben entradas similares y proyectan sus axones hacia regiones específicas.
El papel clave de los astrocitos en la estabilidad del circuito
Pero las neuronas no trabajan solas. En el cerebro, las células gliales, en particular, los astrocitos—células de soporte del cerebro que ayudan a las neuronas a funcionar correctamente— desempeñan un papel fundamental en la estabilidad estructural y en la maduración sináptica.
Cuando los investigadores crearon nodos formados únicamente por neuronas, observaron que las agregaciones tendían a contraerse y despegarse parcialmente del sustrato. Al incorporar astrocitos derivados también de las iPSC, la morfología cambió: los nodos se mantuvieron más planos, mejor adheridos y con menor densidad celular interna .
Además, la actividad eléctrica medida mediante imágenes de calcio reveló diferencias funcionales. Aunque la frecuencia de disparos espontáneos era similar, las neuronas acompañadas de astrocitos mostraban picos más estrechos, indicativos de potenciales de acción más breves y posiblemente de una maduración funcional más avanzada .
En otras palabras: el soporte glial no solo estabiliza la estructura, sino que también modula la fisiología.
Forzar la direccionalidad del circuito
Una de las innovaciones más interesantes del sistema es el uso de patrones en forma de T en la microtopografía. Estas intersecciones perpendiculares permiten desviar axones hacia direcciones específicas, favoreciendo la construcción de circuitos unidireccionales.
En el diseño óptimo —denominado T3— los axones que llegan a la intersección pueden girar siguiendo los canales horizontales o continuar su trayectoria vertical. Aproximadamente el 45% se alinean con las guías horizontales, mientras que un 30% mantiene la dirección original. Este sesgo es suficiente para concentrar la superposición de prolongaciones en puntos definidos, aumentando la probabilidad de contacto sináptico entre nodos.
Así, los investigadores construyeron circuitos de dos nodos separados, cada uno con poblaciones neuronales distintas —por ejemplo, marcadas con proteínas fluorescentes verdes o rojas— que proyectan sus axones hacia una zona común.
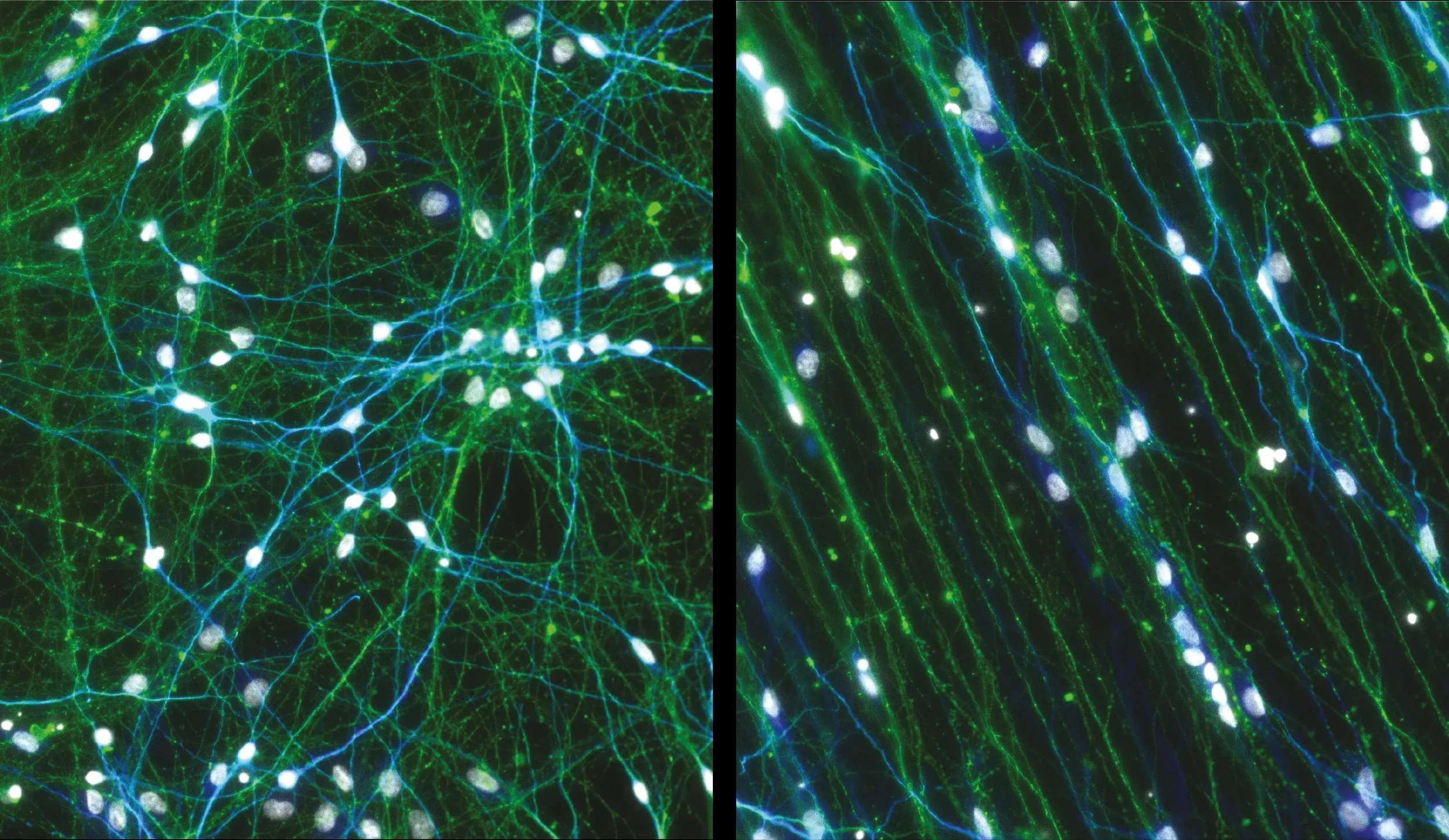
Mediante moldes impresos en 3D, los investigadores crearon polímeros biocompatibles que guían el crecimiento neuronal hacia regiones específicas de la placa de cultivo. Izquierda: neuronas cultivadas sin el dispositivo polimérico; derecha: neuronas cultivadas sobre el polímero con microestrías que orientan su organización. Cortesía: King's College London
Confirmación de conectividad sináptica real
Observar axones que se superponen no basta para demostrar conectividad real. El equipo analizó la presencia de PSD95, una proteína característica de la densidad postsináptica. Encontraron un aumento significativo de puntos de PSD95 en la región de intersección del nodo receptor, aproximadamente el doble que en regiones de control . Además, la colocalización con sinaptofisina —un marcador presináptico— confirmó la existencia de contactos sinápticos físicos.
Una ventaja decisiva del sistema abierto es que permite extraer material de regiones específicas del circuito para llevara a cabo análisis proteómicos, que permiten identificar y cuantificar todas las proteínas presentes en una célula o tejido. Tras veintiocho días de cultivo, los investigadores aislaron proteínas de distintas zonas (nodos y uniones) y realizaron espectrometría de masas.
El análisis de componentes principales mostró que la región donde se forman sinapsis entre nodos presentaba un perfil proteico distinto, enriquecido en términos relacionados con la zona activa presináptica y la sinapsis glutamatérgica. Este nivel de resolución espacial sería difícil de alcanzar en dispositivos microfluídicos cerrados.
Optogenética: control funcional del circuito con luz
La prueba funcional llegó mediante optogenética, una técnica que permite controlar la actividad de neuronas usando luz: ee introducen en las células proteínas sensibles a la luz y, al iluminarlas, se pueden activar o desactivar con gran precisión.
En uno de los nodos, las neuronas expresaban ChrimsonR, un canal iónico sensible a la luz roja. Al aplicar pulsos de 585 nanómetros, estas células generaban potenciales de acción. La actividad se monitorizó con un indicador de calcio.
Tras la estimulación, las neuronas del nodo emisor mostraron respuestas sincronizadas con los pulsos luminosos. Lo más relevante fue que las neuronas del nodo receptor, que no expresaban el canal optogenético, también modificaron su patrón de disparo con un ligero retraso temporal.
Esa latencia sugiere transmisión sináptica funcional entre nodos.
Por qué BioConNet es relevante para el futuro de la neurociencia
El sistema no reproduce la complejidad completa del cerebro y comparte el medio de cultivo entre todos los nodos, lo que limita ciertos experimentos con gradientes químicos. Pero ofrece una combinación inédita de control arquitectónico, accesibilidad molecular y manipulación funcional.
En enfermedades neurodegenerativas, la pérdida de conectividad precede a la muerte neuronal. Poder recrear circuitos humanos definidos, alterar selectivamente uno de los nodos —por ejemplo, con células derivadas de un paciente— y analizar cómo cambia la sinapsis o el perfil proteico abre nuevas vías para estudiar los mecanismos de la desconexión cerebral.
Más que un simple cultivo, BIOCONNET funciona como una plataforma modular donde la conectividad puede diseñarse, observarse y desmontarse. Una placa de circuito biológico que acerca un poco más el laboratorio al cerebro humano real.
«Es importante para nosotros que la plataforma que desarrollamos tenga el máximo impacto posible. Por eso todos los materiales y el diseño se ofrecen como código abierto, haciéndolos completamente reproducibles», concluye Serio.▪️(1-marzo-2026)
Información facilitada por el King's College de Londres
Fuente: Pacharaporn Suklai, Taylor Minckley, Cathleen Hagemann, Karolina Faber, Rosalind Norkett, Ludovica Guetta, Kelly O'Toole, Bethany Geary, Michael J. Devine, Andrea Seri. Engineering Cortical Networks: An Open Platform for Controlled Human Circuit Formation and Synaptic Analysis In Vitro. Advanced Healthcare Materials (2025). DOI: https://doi.org/10.1002/adhm.202500857